Dal Microbiota intestinale al Sesto Senso
|
Getting your Trinity Audio player ready...
|
Il Microbiota intestinale
Il microbiota è l’insieme di microrganismi (batteri, virus, lieviti, funghi, protozoi) che vive in simbiosi nel nostro corpo, principalmente nell’intestino. Composto da circa 100 trilioni di microbi, pesa 1,5-2 kg e svolge funzioni cruciali: un vero e proprio ecosistema complesso e personalizzato, costituito principalmente da microrganismi in equilibrio dinamico tra loro e con l’ospite, che non si limitano a sfruttare le risorse energetiche introdotte con l’alimentazione, ma che hanno la capacità di influenzare l’intero organismo: il nostro metabolismo, il nostro sistema di difesa, il nostro stato di salute, il funzionamento del sistema nervoso centrale e perfino il nostro benessere psicologico è regolato dal cosiddetto “asse intestino-cervello”.
Il microbioma indica invece l’intero patrimonio genetico espresso da tali microrganismi.
Sebbene presente su pelle, cavo orale e polmoni, la concentrazione maggiore si trova nell’intestino (microbiota intestinale).
Il microbiota intestinale inizia a formarsi al momento del parto, definendo la sua composizione “di base” nei primi 12 mesi dopo la nascita, per arrivare a un assetto simile a quello che sarà poi mantenuto in età adulta entro i 3 anni di vita. Nella prima fase del suo sviluppo, la composizione del microbiota è determinata dalla genetica individuale e dai microrganismi materni con i quali il neonato entra in contatto mentre attraversa il canale vaginale (in caso di parto naturale) e nei primi mesi di vita, anche in funzione del tipo di allattamento e svezzamento. Ciò fa sì che ogni individuo sia dotato di un microbiota intestinale unico e non riproducibile, che può essere considerato una vera e propria “impronta digitale microbica”.
Tuttavia, la composizione della microflora endogena non è “rigida”, ma cambia nel corso della vita, adattandosi via via alle sollecitazioni provenienti dall’ambiente esterno (alimentazione, farmaci assunti, cambiamenti di stile di vita, ecc.) e dal nostro stesso organismo (età, oscillazioni ormonali, stress, stati di malattia ecc.). Questa “plasticità” funzionale è legata all’enorme numero di geni che costituiscono il patrimonio genetico microbico intestinale (microbioma), di gran lunga più ricco e diversificato dell’intero genoma umano (si stimano circa 10 milioni di geni batterici vs 23.000 geni umani totali).
Il microbiota è presente lungo tutto l’intestino, ma con sostanziali differenze di abbondanza e diversità dei ceppi batterici ospitati nei vari tratti. In condizioni fisiologiche, la microflora endogena è meno “rigogliosa” nell’intestino tenue, mentre diventa molto più abbondante a livello del colon, dove trova un ambiente particolarmente favorevole per la propria proliferazione. Nel canale intestinale il microbiota interagisce, oltre che con il materiale contenuto nel lume, anche con lo strato più esterno del muco che ne riveste le pareti, di cui contribuisce a definire composizione e caratteristiche, partecipando alla formazione della “barriera intestinale”.
Quando le specie batteriche che compongono il microbiota sono in equilibrio tra loro e con il corpo umano, si dice che è presente uno stato di “eubiosi”. Questa condizione non fa riferimento a un insieme di microrganismi intestinali ben definito, ma a tutte le possibili combinazioni microbiche che, pur variando leggermente, permettono a un certo individuo di trovarsi in uno stato di benessere.
Quando i cambiamenti di composizione del microbiota sono più marcati si parla invece di “disbiosi”, uno stato che equivale alla sostanziale perdita dell’equilibrio dell’ecosistema microbico che impedisce all’intestino di funzionare correttamente, con ripercussioni negative su tutto l’organismo. Generalmente, l’insorgenza di disbiosi si associa a disturbi enterici come gonfiore, crampi, meteorismo, flatulenza, diarrea o stitichezza, nausea/vomito, inappetenza, senso di malessere ecc. La disbiosi è responsabile di un’infiammazione cronica silente, causata proprio da un disequilibrio tra batteri “buoni” e “cattivi, alla base di molte malattie.
L’equilibrio della microflora enterica è pertanto cruciale per garantire la funzionalità del tratto gastrointestinale e il benessere dell’intero organismo attraverso molteplici meccanismi.
In primo luogo, la popolazione batterica intestinale partecipa alla digestione e all’assorbimento dei nutrienti assunti con l’alimentazione. In aggiunta, il microbiota supporta la corretta nutrizione dell’organismo attraverso la produzione di sostanze utili, come alcune vitamine essenziali (soprattutto, vitamine del gruppo B e vitamina K) e altri composti di origine batterica coinvolti nella regolazione dell’attività metabolica (in particolare, gli acidi grassi a catena corta o SCFA, Short Chain Fatty Acid).
Il microbiota intestinale sano è fondamentale anche per il buon funzionamento del sistema immunitario locale e per la prevenzione dell’infiammazione del tratto gastrointestinale e dell’intero organismo, grazie alla sua capacità di proteggere e ripristinare la “funzione barriera” della mucosa intestinale. Questa barriera fisiologica, costituita dallo strato di muco che riveste l’epitelio intestinale e dall’epitelio stesso, impedisce ai microrganismi contenuti nel lume di entrare in diretto contatto con gli strati più profondi delle pareti dell’intestino e di sollecitare in modo abnorme il sistema immunitario locale.
Inoltre, la barriera intestinale blocca il passaggio nel sangue di microbi potenzialmente patogeni e sostanze dannose, contribuendo alla prevenzione di infezioni sistemiche ed effetti tossici, e riduce l’assorbimento di composti sensibilizzanti introdotti con l’alimentazione (allergeni), diminuendo la probabilità di sviluppare allergie, soprattutto nei bambini.
Il microbiota intestinale svolge un ruolo fondamentale nella difesa dalle infezioni del tratto gastrointestinale attraverso diversi meccanismi, come la produzione di batteriocine (piccole proteine prodotte da alcuni batteri intestinali capaci di uccidere altri batteri), perossido di idrogeno e altre molecole in grado di contrastare la proliferazione di specie batteriche e protozoi potenzialmente dannosi per l’organismo.
Infine, è stato dimostrato che la microflora enterica può influenzare il benessere e le funzioni di altri organi e apparati, come la pelle, le vie urinarie, l’apparato genitale femminile, il fegato e il sistema nervoso centrale. Negli ultimi anni, gli studi su quest’ultimo fronte si stanno moltiplicando in seguito all’evidenza che alcuni composti prodotti dai batteri intestinali possono raggiungere il cervello attraverso il sangue o le terminazioni del nervo vago (“asse intestino-cervello”) e contribuire, così, a modulare il tono dell’umore, la risposta allo stress e il rischio di sviluppare patologie neurodegenerative, come la malattia di Parkinson o di Alzheimer.
Tra i fattori capaci di influenzare l’equilibrio del microbiota la dieta è, senza dubbio, la variabile in grado di incidere maggiormente sulla microflora enterica, in senso positivo o negativo, al punto che è stato dimostrato che le persone che seguono un’alimentazione basata prevalentemente su cibi semplici di origine vegetale (frutta, verdura, cereali) hanno un profilo microbico intestinale differente e più stabile di chi segue abitualmente una dieta di tipo occidentale (ricca di zuccheri semplici, grassi saturi e proteine animali), che predispone alle disbiosi.
Un altro fattore chiave che influenza la ricchezza e la composizione del microbiota intestinale è una corretta attività fisica (ossia moderata, regolare e commisurata alle potenzialità individuali), mentre sia la sedentarietà sia lo sforzo fisico molto intenso (per esempio, quello necessario per una maratona) rendono maggiormente soggetti ad alterazioni del microbiota (disbiosi).
Alimentazione e livello di attività fisica hanno anche effetti indiretti sulle popolazioni batteriche intestinali, per le ripercussioni che possono avere sul peso corporeo e, conseguentemente, sull’equilibrio metabolico e ormonale. In particolare, è stato osservato che condizioni di forte sovrappeso e obesità si associano a una microflora enterica meno ricca e meno stabile, quindi più propensa a dar luogo disturbi e diverse patologie, sia gastrointestinali sia di tipo sistemico (a partire da diabete di tipo 2 e malattie cardiovascolari).
Effetti destabilizzanti più o meno marcati sull’equilibrio del microbiota intestinale possono essere, poi, determinati dall’assunzione di diversi tipi di farmaci, a breve o lungo termine, per la terapia di una malattia acuta o di condizioni croniche di varia natura.
I medicinali a maggior rischio di causare disbiosi severe e conseguenti disturbi intestinali sono senza dubbio gli antibiotici che, anche per questa ragione (oltre che per evitare alterazioni delle difese immunitarie e l’induzione di resistenze batteriche) dovrebbero essere assunti sempre e soltanto dopo una visita medica e gli eventuali esami necessari per verificare le condizioni del paziente e formulare una diagnosi precisa della malattia presente.
Ulteriori sostanze di cui tener conto e preferibilmente da evitare ai fini della tutela della microflora enterica, oltre che di molti organi e apparati del corpo umano, sono il fumo e gli alcolici, entrambi caratterizzati da effetti fortemente destabilizzanti e proinfiammatori a livello del tratto gastrointestinale.
Due fattori “non organici” che possono incidere in modo significativo sull’equilibrio del microbiota intestinale sono lo stress e i disturbi psichiatrici (ansia, depressione ecc.), fortemente implicati anche nello sviluppo e nel peggioramento della sindrome dell’intestino irritabile (Irritable Bowel Syndrome, IBS), una condizione caratterizzata da sintomi come dolore, crampi e gonfiore addominali, meteorismo e flatulenza, diarrea e/o stipsi prevalenti o in alternanza, nella quale è sempre più evidente il ruolo giocato dalle disbiosi.
Stati di ansia, depressione e IBS tendono a interessare più spesso le donne che, durante tutta l’età fertile, devono anche fare i conti anche con periodiche oscillazioni fisiologiche dei livelli ormonali. Studi recenti hanno indicato che gli ormoni femminili (estrogeni) hanno la capacità di influenzare il microbiota, sia in modo diretto (modificando le caratteristiche dell’ambiente che lo ospita e promuovendo l’infiammazione della mucosa intestinale) sia indirettamente (attraverso i cambiamenti transitori del tono dell’umore, dell’alimentazione ecc.).
Seguire una dieta bilanciata, uno stile di vita sano e ritmi regolari è la migliore strategia per proteggere l’equilibrio del microbiota intestinale e promuovere il benessere dell’intero organismo.
Negli individui particolarmente soggetti ad alterazioni della microflora e ai relativi disagi intestinali, lo stato di eubiosi può essere favorito più facilmente attraverso l’assunzione ciclica o a lungo termine di preparati probiotici e/o prebiotici.
Per definizione, i probiotici sono “microrganismi vivi e vitali che, somministrati in quantità adeguata, sono in grado di determinare benefici per la salute di chi li assume”. Il Ministero della Salute ha indicato che questa “quantità adeguata” deve essere pari ad almeno 109 UFC (Unità Formanti Colonia, ossia microrganismi in grado di moltiplicarsi attivamente nell’intestino, almeno transitoriamente) per almeno uno dei ceppi batterici presenti nella porzione quotidiana del preparato probiotico. In commercio esistono sia prodotti mono-ceppo (ossia contenenti un solo tipo di microrganismo probiotico) sia prodotti multi-ceppo (ossia contenenti più tipi differenti di microrganismi probiotici, in quantità uguale o diversa).
I prebiotici, invece, sono sostanze non digeribili dall’intestino umano, ma che possono essere fermentate da alcune specie batteriche presenti nel microbiota enterico. In questo modo, i prebiotici favoriscono l’equilibrio del microbiota intestinale. I principali prebiotici in commercio sono l’inulina, i frutto-oligosaccaridi (FOS) e lo psyllium, cui si aggiungono zuccheri a corta catena come il lattulosio e i galatto-oligosaccaridi (GOS).
In alcuni casi, batteri probiotici e composti prebiotici vengono inseriti nello stesso prodotto: preparati di questo tipo vengono chiamati “simbiotici”.
Attualmente, sono disponibili in commercio innumerevoli preparati e integratori alimentari probiotici mono-ceppo o multiceppo, prebiotici e simbiotici, con caratteristiche e proprietà differenti. Per essere certi di scegliere quello più adatto alle proprie necessità, è consigliabile farsi indirizzare nell’acquisto dal medico di famiglia o dal farmacista.
I cibi fermentati sono ottimi alleati del microbiota intestinale, poiché arricchiscono la flora batterica con microrganismi benefici, aumentandone la biodiversità e riducendo l’infiammazione. Alimenti come yogurt, kefir, crauti, miso e tempeh contengono probiotici che, consumati regolarmente, sostengono il sistema immunitario, migliorano la digestione e l’assorbimento dei nutrienti.
Il “sesto senso” batterico
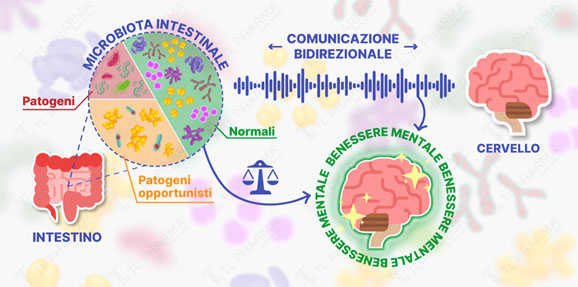
Il microbiota è al centro dell’asse asse intestino-cervello. Le nuove conoscenze in questo campo evidenziano l’esistenza di comunicazioni bidirezionali estremamente complesse e dinamiche, dove il microbiota intestinale gioca un ruolo da protagonista nella salute mentale e fisica. In particolare, recenti ricerche (2024-2025) hanno approfondito il modo in cui i microrganismi intestinali influenzano il cervello attraverso vie immunitarie, endocrine e neurali, aprendo nuove prospettive terapeutiche ed hanno consentito di identificare quello che viene definito “sesto senso” batterico.
Il “sesto senso” batterico, o senso neurobiotico, è un meccanismo scoperto nel 2025 attraverso il quale l’intestino rileva i segnali dei batteri, influenzando in tempo reale appetito, metabolismo e umore. Le cellule neuropodi nell’intestino percepiscono la flagellina batterica e inviano segnali al cervello via nervo vago, agendo come un dialogo diretto tra microbiota e sistema nervoso. In particolare, i batteri intestinali producono flagellina, una proteina che attiva il recettore TLR5 nelle cellule neuropodi, inviando messaggi al cervello. Questo sistema neurobiotico agisce sul nervo vago per comunicare sazietà o fame al cervello, influenzando il controllo del peso corporeo. Pertanto, un’alterazione di questo “sesto senso” può portare a disturbi del comportamento alimentare, obesità e alterazioni dell’umore. E’ questa conferma che il microbiota intestinale dialoga direttamente con il sistema nervoso centrale, influenzando non solo la digestione ma anche le funzioni cognitive ed emotive. Un’alimentazione ricca di fibre e uno stile di vita sano sono fondamentali per sostenere questo sistema e mantenere l’equilibrio tra i microbi intestinali e il cervello.
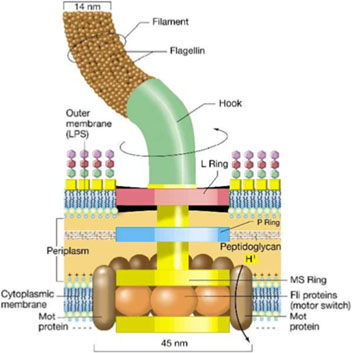 La parte centrale di questa storia è una molecola chiamata flagellina, una proteina presente principalmente nel flagello batterico, una sorta di coda che permette ai batteri di nuotare un po’ come succede per gli spermatozoi, immagine più nota nell’immaginario collettivo. È una proteina molto antica: la maggior parte dei batteri possiede infatti questa struttura, risultato di milioni di anni di evoluzione. Alcuni batteri del nostro microbiota intestinale rilasciano la flagellina, soprattutto dopo un pasto, e alcune cellule altamente specializzate, chiamate neuropodi, sono in grado di percepirne la presenza grazie a un recettore specifico: il TLR5 (Toll-like receptor 5). L’attivazione di questo recettore stimola il rilascio di un ormone, il peptide YY, che attiva un circuito nervoso diretto al cervello tramite le fibre del nervo vago, trasmettendo un segnale di soppressione dell’appetito. Questa comunicazione, molto rapida, costituisce un asse intestino-cervello, che i ricercatori hanno definito come “senso neurobiotico”: un sesto senso, distinto dalla percezione gustativa e sensoriale, che permetterebbe al cervello di rispondere in tempo reale ai messaggi inviati dai microbi intestinali, regolando così i comportamenti alimentari e influenzando le decisioni relative alla nutrizione e all’assunzione di cibo.
La parte centrale di questa storia è una molecola chiamata flagellina, una proteina presente principalmente nel flagello batterico, una sorta di coda che permette ai batteri di nuotare un po’ come succede per gli spermatozoi, immagine più nota nell’immaginario collettivo. È una proteina molto antica: la maggior parte dei batteri possiede infatti questa struttura, risultato di milioni di anni di evoluzione. Alcuni batteri del nostro microbiota intestinale rilasciano la flagellina, soprattutto dopo un pasto, e alcune cellule altamente specializzate, chiamate neuropodi, sono in grado di percepirne la presenza grazie a un recettore specifico: il TLR5 (Toll-like receptor 5). L’attivazione di questo recettore stimola il rilascio di un ormone, il peptide YY, che attiva un circuito nervoso diretto al cervello tramite le fibre del nervo vago, trasmettendo un segnale di soppressione dell’appetito. Questa comunicazione, molto rapida, costituisce un asse intestino-cervello, che i ricercatori hanno definito come “senso neurobiotico”: un sesto senso, distinto dalla percezione gustativa e sensoriale, che permetterebbe al cervello di rispondere in tempo reale ai messaggi inviati dai microbi intestinali, regolando così i comportamenti alimentari e influenzando le decisioni relative alla nutrizione e all’assunzione di cibo.
Per giungere a queste conclusioni sono stati utilizzati topi di laboratorio, tenuti a digiuno per una notte intera, ai quali è stata poi iniettata una dose di flagellina nell’intestino. Osservando le quantità di cibo consumato al risveglio, gli studiosi hanno notato che questi topi mangiavano di meno rispetto a quelli non esposti alla flagellina, suggerendo che la presenza di questa proteina possa contribuire a modulare l’appetito. Hanno poi ripetuto l’esperimento con topi transgenici, modificati geneticamente, nei quali il recettore TLR5 era stato rimosso: questi animali mangiavano pasti più abbondanti e tendevano ad aumentare di peso, risultando in una regolazione dell’appetito compromessa. Questo sistema di controllo agisce in modo separato dalle risposte immunitarie o dal metabolismo intestinale: si tratta di un segnale distinto, indipendente, diverso dagli altri meccanismi di difesa attivati in risposta a segnali di infiammazione, spesso associati a squilibri della flora batterica intestinale.
Al momento questi risultati sono stati osservati solo nei topi, e non si può ancora dire con certezza se e in che misura siano applicabili all’essere umano, considerando le importanti differenze tra le due specie. Tuttavia, questa scoperta apre a nuove prospettive di ricerca, che potrebbero portare allo sviluppo di interventi innovativi nel trattamento di condizioni legate all’alimentazione, come obesità e disturbi del comportamento alimentare. Se si confermasse anche negli esseri umani, ciò potrebbe rivoluzionare il nostro modo di concepire le cause e individuare nuove soluzioni a problematiche di salute pubblica, implementando approcci o diete più olistiche che tengano in considerazione anche il microbiota.
Liu WW, Reicher N, Alway E, Rupprecht LE, Weng P, Schaefgen C, Klein ME, Villalobos JA, Puerto-Hernandez C, Kiesling Altún YG, Carbajal A, Aguayo-Guerrero JA, Coss A, Sahasrabudhe A, Anikeeva P, de Araujo A, Bali A, de Lartigue G, Gil-Lievana E, Gutierrez R, Miao EA, Rawls JF, Kaelberer MM, Bohórquez DV. A gut sense for a microbial pattern regulates feeding. Nature. 2025 Sep;645(8081):729-736. doi: 10.1038/s41586-025-09301-7. Epub x2025 Jul 23. PMID: 40702192; PMCID: PMC12443592.






