Il microbiota intestinale
|
Getting your Trinity Audio player ready...
|
Il microbiota intestinale (termine che ha via via sostituito quello di “flora intestinale”) è l’insieme dei microrganismi, prevalentemente batteri, ma anche funghi e virus, che convivono e interagiscono con l’organismo umano senza danneggiarlo, ma stabilendo una simbiosi mutualistica.
Il termine microbioma indica invece la totalità del patrimonio genetico posseduto dal microbiota, cioè i geni che quest’ultimo è in grado di esprimere.
Il sistema nervoso enterico (SNE)
Cervello e intestino sono strettamente correlati; di più parlano lo stesso linguaggio e usano gli stessi mediatori per originare delle reazioni e ottenere risposte agli stimoli.
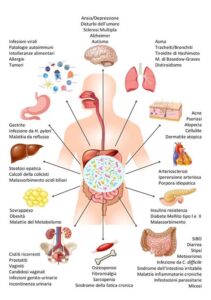 L’apparato gastrointestinale è un organo decisamente complesso: affinché la digestione e l’assorbimento dei cibi possano aver luogo si devono verificare una serie di eventi, a partire dalla masticazione nella bocca fino all’espulsione degli scarti con le feci. Nel mezzo, ad orchestrare il tutto, vi è il sistema nervoso enterico (SNE) che regola e coordina tutte le funzioni che si susseguono. Il sistema nervoso enterico è la più grande e complessa delle tre componenti del sistema nervoso autonomo dell’essere umano; le altre due sono il sistema simpatico e il parasimpatico: i tre sistemi, insieme, sono deputati al controllo del funzionamento dei muscoli degli organi interni, come, per esempio, dei muscoli del cuore e aiutano il corpo a riposare, rilassarsi, digerire il “cibocervello” e a reagire a situazioni di emergenza con il classico comportamento di “attacco o fuga”.
L’apparato gastrointestinale è un organo decisamente complesso: affinché la digestione e l’assorbimento dei cibi possano aver luogo si devono verificare una serie di eventi, a partire dalla masticazione nella bocca fino all’espulsione degli scarti con le feci. Nel mezzo, ad orchestrare il tutto, vi è il sistema nervoso enterico (SNE) che regola e coordina tutte le funzioni che si susseguono. Il sistema nervoso enterico è la più grande e complessa delle tre componenti del sistema nervoso autonomo dell’essere umano; le altre due sono il sistema simpatico e il parasimpatico: i tre sistemi, insieme, sono deputati al controllo del funzionamento dei muscoli degli organi interni, come, per esempio, dei muscoli del cuore e aiutano il corpo a riposare, rilassarsi, digerire il “cibocervello” e a reagire a situazioni di emergenza con il classico comportamento di “attacco o fuga”.
Questo sistema nell’uomo è composto da oltre 100 milioni di neuroni (una quantità addirittura superiore a quella dei neuroni presenti nella spina dorsale) che, dal nostro intestino, innervano l’intero tratto gastrointestinale.
Il ruolo della rete organizzata dai neuroni enterici è:
- contribuire alla motilità gastrointestinale, coordinando i muscoli lisci di stomaco e intestino;
- assorbire i nutrienti;
- produrre gli acidi gastrici;
- sovraintendere e coordinare le diverse funzioni digestive.
Se per il controllo di tutte queste funzioni intestinali fosse necessario il pensiero cosciente, in realtà, ci rimarrebbe ben poco tempo per fare altro nella vita, ma l’evoluzione ha dotato il nostro “secondo cervello” della capacità di gestire il tratto gastrointestinale in autonomia senza il controllo del sistema nervoso centrale.
L’asse microbiota – intestino – cervello
Quindi, nonostante il sistema nervoso enterico sia in grado di funzionare, per quanto riguarda le funzioni digestive di base, anche senza ricevere segnali dal cervello, normalmente cervello e intestino lavorano insieme, attraverso un fitto scambio di comunicazioni bi-direzionali lungo l’asse intestino-cervello.
In questo flusso di comunicazioni svolge un ruolo importante il microbiota intestinale, cioè gli oltre 100 trilioni di microorganismi che vivono nell’intestino e con i quali abbiamo instaurato una relazione simbiotica. Il microbiota intestinale regola l’equilibrio intestinale ed extra-intestinale.
Inoltre, sempre più prove scientifiche sottolineano il ruolo del microbiota, oltre che nelle infiammazioni croniche dell’intestino, in disturbi neuropsichiatrici, nell’obesità, nel morbo di Parkinson.
L’idea che l’intestino influenzi il cervello, e di conseguenza anche il comportamento, è ampiamente riconosciuta e condivisa. Appare ormai sempre più evidente che i microbi dell’intestino contribuiscono a plasmare il normale sviluppo neurale, la biochimica del cervello e il comportamento. In altri termini, il microbiota intestinale rappresenta l’elemento nodale nella comunicazione tra l’intestino e il cervello. Tutto ciò ha portato anche alla creazione di una nuova disciplina: la psico-neuro-endocrino-immunologia (PNEI), che si occupa di studiare le connessioni tra detti sistemi. Questi grandi sistemi di regolazione biologica scambiano informazioni tra loro e vengono influenzati dagli stati psicologici.
In effetti, il microbiota pare possa mediare la comunicazione tra intestino e cervello attraverso diverse vie di comunicazione che includono il sistema endocrino, immunitario, metabolico (tramite la produzione di neurotrasmettitori come la serotonina) oppure con il coinvolgimento del sistema nervoso autonomo e del nervo vago nello specifico. Interlocutori di primo piano nella comunicazione intestino-cervello sono: il nervo vago e la serotonina.
Il nervo vago, il decimo delle dodici paia di nervi cranici che consentono al sistema nervoso centrale di comunicare con gli organi periferici dell’organismo, è il principale componente del sistema nervoso parasimpatico. Il microbiota può attivare le comunicazioni dall’intestino al cervello utilizzando questo canale. Il nervo vago è in grado di recepire le molecole prodotte dai batteri e di trasferirle al sistema nervoso centrale per aiutarlo a produrre una risposta che, se inappropriata, può portare alla manifestazione di diversi disturbi del tratto gastrointestinale.
Fattori stressanti possono inibire l’attività del nervo vago e avere conseguenze sul sistema digerente e sulla composizione del microbiota. Un tono vagale basso è stato osservato in pazienti affetti da sindrome del colon irritabile e nelle malattie infiammatorie croniche intestinali.
Alla comunicazione lungo l’asse partecipa anche la serotonina, un neurotrasmettitore prodotto per il 95% dal SNE e presente anche nel sistema nervoso centrale. Nell’intestino questa molecola è coinvolta nella regolazione della secrezione e della motilità gastrointestinali e nella percezione del dolore, mentre nel sistema nervoso centrale è implicata nella regolazione del tono dell’umore. Disfunzioni a livello del sistema che regola la quantità di serotina in circolo, possono portare a problemi del tratto gastrointestinale e a disturbi dell’umore.
Il microbiota può regolare la sintesi nell’intestino di questo neurotrasmettitore; questa comunità batterica potrebbe avere un ruolo importante nella disponibilità e nel metabolismo del triptofano, un amminoacido da assumere con la dieta e precursore della serotonina.
Caratteristiche del microbiota umano
Il microbiota gastrointestinale umano è caratterizzato da
- Diversità individuale in relazione a:
- Profilo genetico dell’ospite
- Età
- Stato di salute
- Esposizione ambientale
- Dieta
- Esposizione ad agenti chimici/farmaci
- Stili di vita
- Stabilità
- Il microbiota possiede uno stato di equilibrio rappresentato da un nucleo di microrganismi (cuore del microbiota) che malgrado i cambiamenti temporali dei singoli microrganismi gli permette di mantenere l’importante ruolo di protezione immune, di produzione ed assimilazione dei nutrienti.
- Capacità di recupero (Resilience)
– Il microbiota alterato da vari fattori di disturbo ha la capacità di recuperare il proprio stato di equilibrio nel tempo o un nuovo stato mantenendo le proprie funzioni.
Un ruolo cruciale nella composizione e distribuzione del microbiota intestinale è svolto dal tipo di dieta seguito.
Una dieta ricca in carboidrati non glicemici (le cosidette “fibre alimentari”) facilita la presenza di Bifidobatteri e Lattobacilli, mentre un’alimentazione ricca di grassi e carne aumenta la presenza dei batteri putrefattori che possono portare alla formazione di sostanze cancerogene. Numerose ricerche, infatti, hanno dimostrato l’associazione tra la prevalenza di alcuni batteri e BMI, DM2 e obesità, proprio perché il microbiota può aumentare l’estrazione energetica dal cibo, modificare le vie metaboliche dell’ospite, provocare un’infiammazione cronica di basso grado, aumentare l’insulino-resistenza, influenzare la secrezione di ormoni intestinali (incretine), e la motilità intestinale.
Una dieta iperlipidica e povera in fibre cambia il microbiota in modo complesso e specificamente riduce i Bifidobatteri, promuove endotossiemia metabolica e provoca lo sviluppo di disordini metabolici tramite un meccanismo dipendente CD14/TLR4. La riduzione dei Bifidobatteri è associata a un più alto livello plasmatico di LPS (endotoxemia metabolica), alla secrezione di citochine proinfiammatorie LPS-dipendenti.
Inoltre dieta iperlipidica e LPS promuovono uno stato infiammatorio di basso grado e disordini metabolici indotti (insulino-resistenza, diabete, obesità, steatosi, infiltrazione macrofagica del tessuto adiposo).
Uno studio su oltre 23 mila persone ha dimostrato che chi mangia abitualmente una minore quantità di fibre risulta essere più colpito da obesità, sindrome metabolica, infiammazione generalizzata. Anche i grassi alimentari influenzano quantità e tipo di microbiota, soprattutto gli omega 3 con effetto protettivo. Sono stati identificati prebiotici (fruttoligosaccaridi e galattooligosaccaridi), capaci di stimolare mediante popolazioni saccarolitiche la produzione di SCFA (propionato e butirrato) che hanno molteplici ruoli in obesità, DM2 e patologie infiammatorie intestinali. L’apporto di probiotici, in particolare Akkermansia muciniphila, può ridurre obesità e diabete di tipo 2.
Un maggior consumo, infine, di latticini ipolipidici, soprattutto yogurt, è associato con un ridotto rischio di sviluppo di DM2.
Cambiare tipo di alimentazione modifica velocemente, molto più velocemente del previsto, la flora batterica intestinale, in entrambi i sensi.
Le ormai rare popolazioni di cacciatori-raccoglitori, come gli Hadza (gruppo etnico della Tanzania che vive attorno al lago Eyasi. La popolazione raggiunge quasi le mille persone; 300-400 vivono come cacciatori-raccoglitori), hanno una flora intestinale differente da quella delle popolazioni occidentali: è più varia, differisce fra uomini e donne, e contiene batteri in grado di demolire fibre indigeribili ed è carente di ceppi solitamente considerati anti-obesità, in relazione alle loro condizioni di vita.
Il trapianto di feci compatibili geneticamente da soggetti magri a soggetti obesi rappresenta una nuova possibilità terapeutica nell’obesità resistente alle comuni terapie.
Funzioni del microbiota
- rappresenta la nostra prima fonte di difesa (barriera) verso gli attacchi esterni: i microrganismi “buoni” presenti nell’intestino combattono quelli “cattivi” che arrivano dall’esterno attraverso la produzione di antibiotici naturali, la competizione con i nutrienti e per gli spazi, l’amensalismo, l’adesione delle cellule epiteliali intestinali, etc., o altri meccanismi d’azione (“crowiding out” o «effetto di spiazzamento»; elaborazione e la secrezione di peptidi antimicrobici; azioni favorenti l’integrità dell’epitelio intestinale; anticorpi IgA, etc.);
- regola il nostro sistema immunitario, “insegnandogli” a modulare la risposta immunitaria mantenendo l’omeostasi e la natura mutualistica con la comunità di microbi residenti nel nostro organismo; in sostanza fa sì che il nostro sistema di difesa reagisca in modo consono all’attacco ricevuto. Vi sono oggi pochi dubbi sul fatto che il sistema immunitario dell’uomo dipenda strettamente dalle istruzioni che riceve continuamente dal suo microbiota: se questa comunità di simbionti perde in ricchezza e diversità, e va incontro a quel processo che viene definito “disbiosi”, il sistema immunitario dell’ospite inizia a perdere di efficacia e precisione al punto da reagire in maniera incongrua, per eccesso, per difetto, o talora contro l’oggetto sbagliato (come avviene nelle malattie autoimmuni).
- regola il metabolismo, per cui svolge un ruolo essenziale nel nostro normotipo (ovvero sul peso dell’organismo) grazie a digestione di polisaccaridi complessi con produzione di acidi grassi a catena corta, sintesi di vitamine e aminoacidi, regolazione dell’insulino-resistenza, metabolismo del colesterolo, detossicazione di xenobiotici (cioè di sostanze sintetiche o naturali estranee al nostro organismo)
- svolge una funzione neuroendocrina, con influenza su motilità, modalità sensorie e secretive del tratto gastrointestinale. Non a caso le cellule dell’intestino producono il 95% della serotonina, il neurotrasmettitore del benessere.
- produce sostanze importantissime, come gli acidi grassi a catena corta che proteggono le nostre pareti intestinali dall’infiammazione e vitamine del gruppo B e la vitamina K
- esercita una funzione farmaco-micro-biomica, con un ruolo nella biodisponibilità, efficacia e tossicità di farmaci assunti.
Le alterazioni del microbiota
Un microbiota sano è un requisito essenziale per un organismo sano. Si parla di eubiosi microbiotica quando tra microbiota e organismo umano esiste una condizione di equilibrio che porta all’esecuzione di funzioni complesse con vantaggio reciproco. Si parla, invece, di disbiosi microbiotica quando esiste una condizione di squilibrio numerico e qualitativo del microbiota per cui si altera la barriera intestinale, viene meno la sintesi di molecole utili e microrganismi patogeni presenti metabolizzano composti dannosi all’organismo. Si determinano, così, una endotossiemia, cioè una traslocazione batterica o di componenti batterici, e una infiammazione cronica sistemica di basso grado con aumento in circolo di sostanze proinfiammatorie.
Un cambiamento nella popolazione microbica con prevalenza delle specie potenzialmente dannose è alla base della disbiosi e può determinare l’insorgere di varie patologie: diarrea, malattie infiammatorie croniche IBD, obesità, diabete, neoplasie Il ripristino di un equilibrio con l’introduzione di probiotici, prebiotici e simbiotici sembra in grado di prevenire e curare molte di tali manifestazioni patologiche.
| Negli individui sani, la composizione del microbiota intestinale è estremamente diversificata, con i ceppi batterici protettivi in quantità superiori rispetto a quelli potenzialmente dannosi. Questa composizione assicura una divisione efficiente e benefica delle attività che si svolgono nell’intestino. La perdita di questa diversificazione, o una restrizione della diversità, unita alla comparsa di squilibri tra le proporzioni dei ceppi batterici, può avere gravi conseguenze. Questa perdita di equilibrio, chiamata disbiosi, è associata a una vasta gamma di disturbi. Tra questi, diarrea, sindrome del colon irritabile (IBS) o malattia infiammatoria dell’intestino (IBD), tumore del colon retto e anche alcune patologie epatiche e allergie, nonché malattie collegate all’alimentazione come sindrome metabolica, obesità, diabete di tipo 2 o celiachia. Le composizioni alterate del microbiota intestinale hanno effetti anche sul sistema nervoso centrale, perché intestino e cervello sono connessi da una moltitudine di pathway di comunicazione utilizzati da trasmettitori e metaboliti batterici. Non sorprende, quindi, che persino disturbi mentali e dello sviluppo neurologico come la depressione, l’ansia e l’autismo possano essere collegati alla disbiosi del microbiota intestinale. Una riduzione della diversificazione microbica nell’intestino è accompagnata dall’instabilità dell’ecosistema formato da questi micro-organismi interagenti: una composizione disbiotica del microbiota cambia molto più di frequente di una composizione sana e la sua resilienza si indebolisce, il che significa una capacità di recupero notevolmente rallentata o persino insufficiente dopo una diarrea o l’assunzione di farmaci antibiotici. |
Una condizione di disbiosi intestinale può essere determinata da:
- l’utilizzo di farmaci: rappresenta sicuramente la prima causa; gli antibiotici non uccidono solo i batteri cattivi, ma anche buona parte dei batteri buoni creando un grandissimo scompenso nel nostro microbiota; agenti come gli anti-infiammatori steroidei possono uccidere i batteri buoni e promuovere lo sviluppo di batteri patogeni
- il tipo di alimentazione: è questa un’altra causa primaria; in effetti è ormai dimostrato che l’alimentazione influisce sulla composizione del nostro microbiota. Un’alimentazione ricca di prodotti raffinati (farina bianca in primis), zucchero bianco e di oli vegetali ricchi di omega 6 (olio di girasole, arachidi, cartamo, soia ecc. contenuti nei prodotti da forno preconfezionati) riduce la quantità di batteri buoni, favorendo il proliferare di specie patogene (batteri cattivi). Un’alimentazione ricca di proteine stimola, invece, la produzione di sostanze infiammatorie a livello intestinale. Un’alimentazione vegetariana e ricca di carboidrati complessi è verosimilmente quella più gradita al nostro microbiota;
- episodi di diarrea (v. anche abuso di lassativi) che portano via un sacco di batteri del nostro microbiota;
- malnutrizione, spesso auto-indotta come nei casi dei disturbi dell’alimentazione: i batteri hanno bisogno di cibo e un’alimentazione povera di calorie induce la diminuzione di alcune specie di batteri “buoni”;
- il mangiare troppo: quando si mangia troppo, più di quanto il nostro apparato digerente non sia in grado di digerire, tutto ciò che non viene digerito in modo efficiente diventa cibo per i batteri cattivi che iniziano a proliferare felicemente;
- il consumo di alcol, droghe, tabacco così come l’inquinamento contrastano la crescita di batteri buoni;
- altre cause, fra cui patologie come malattie epatiche, pancreatiche, delle vie biliari o gastriche come l’ipo/acloridria; intolleranze alimentari (celiachia e intolleranza al lattosio); parassitosi intestinali; malattia diverticolare; cause neurogene (stati di ansia, alterazione del ritmo sonno-veglia); alterazioni anatomiche intestinali (come by pass, resezioni intestinali); infine l’utilizzo di acqua del rubinetto contenente un eccesso di cloro.
Grazie a innovative tecniche di sequenziamento del DNA microbiotico è oggi possibile ottenere una descrizione dettagliata della composizione del microbiota intestinale per analizzare il grado di efficienza metabolica e intervenire. L’analisi si effettua raccogliendo un campione fecale. Conoscere la composizione e lo stato del microbiota consente di preservarne l’equilibrio o correggere eventuali condizioni di squilibrio.
Pertanto, è molto importante tenere in equilibrio il microbiota attraverso azioni quali:
- Prediligere un’alimentazione basata su prodotti integrali e naturali
- Consumare tante verdure, soprattutto a foglia verde (meglio se cotte per facilitarne la digestione), cereali integrali e legumi
- Evitare tutti i prodotti raffinati e preconfezionati contenenti farina bianca, zucchero bianco, oli e margarine vegetali (biscotti, crackers, torte, merendine, patatine, salatini, caramelle, bevande gassate ecc.)
- Evitare il consumo di alcol, tabacco e droghe
- Bere acqua senza cloro (filtrata con opportune brocche o in bottiglie di vetro)
- Ridurre il ricorso a farmaci se non strettamente necessari
- Ridurre le condizioni di stress
- Avvalersi di probiotici e psicobiotici per ripopolare la flora batterica
Microrganismi “buoni” e “cattivi”
L’intestino è un organo dell’apparato digerente che svolge un compito importantissimo per il nostro organismo: attraverso la digestione degli alimenti ed il loro assorbimento fornisce i nutrimenti necessari al corpo e si libera dei materiali di scarto e delle tossine.
Alcuni ceppi batterici del microbiota svolgono funzioni benefiche, ma plasmare la flora intestinale modificando l’alimentazione risulta ancora complesso. Innanzitutto, i ceppi indigeni ostacolano la colonizzazione dell’intestino da parte di nuovi microbi, tra cui quelli patogeni; poi, alcuni batteri sintetizzano sostanze utili (per esempio vitamina K) e digeriscono molecole complesse, producendo nuove molecole che possono essere utilizzate dal nostro organismo. Nell’intestino umano risiedono circa 400 tipologie differenti di batteri, prevalentemente bifido batteri (nel colon) e lattobacilli (nell’intestino tenue). Oltre alla flora batterica, troviamo miceti, virus e clostridi che, generalmente, non rivestono un ruolo patogeno. In condizioni normali la flora batterica è in perfetto equilibrio, anzi simbiosi, con l’organismo umano che fornisce ai batteri materiale indigerito per il loro sostentamento: si parla di sostanze prebiotiche. Queste sostanze stimolano la crescita e l’attività dei batteri probiotici, inducendo effetti positivi per la salute umana. I principali prebiotici sono i FOS (frutto-oligosaccaridi), le inuline, il lattitolo, il lattulosio, alcuni oligosaccaridi, le pirodestrine.
Gli acidi grassi a catena corta prodotti dai batteri intestinali, specialmente l’acido butirrico, sono utili a mantenere in salute l’intestino, proteggendolo dalle infiammazioni e dall’insorgenza di tumori. Inoltre, il microbiota mantiene in «allenamento» il sistema immunitario. Un microbiota ricco di batteri capaci di digerire e fermentare i flavonoidi contenuti nella frutta e nella verdura promuove la produzione di sostanze che hanno effetti protettivi sulla salute cardiovascolare.
Cibi ricchi di acidi grassi saturi e alimenti molto calorici stimolano invece la proliferazione di ceppi di batteri che promuovono l’infiammazione. Alcune sostanze prodotte dal microbiota intestinale sembrano coinvolte nella regolazione dell’appetito e nell’aumento di peso. Se la dieta è povera di fibra, diminuisce la popolazione dei Bacterioides, aumenta quella dei Firmicutes e diversi studi suggeriscono che il rapporto tra Bacterioides e Firmicutes sia un fattore importante per l’obesità. In generale, è preferibile un’alta diversità del microbiota, cioè la presenza di molti ceppi microbici diversi.
Teoricamente, arricchendo il microbiota intestinale di batteri «buoni» a scapito dei batteri «cattivi», si dovrebbe promuovere un buono stato di salute. Tuttavia, non può esistere un microbiota ideale uguale per tutti: i geni e le caratteristiche individuali hanno un ruolo determinante.
Studi sull’uso dei prebiotici (sostanze che promuovono la crescita dei batteri «buoni», come per esempio l’inulina) hanno mostrato che la risposta è personale e dipende dalla composizione iniziale del microbiota intestinale. L’industria dei probiotici è in fiorente attività, eppure i dati sull’efficacia dei probiotici in condizioni patologiche non sono consistenti tra loro, a indicare che non si tratta di un tipo di intervento generalizzabile. Plasmare il microbiota solo modificando l’alimentazione appare ancora molto complicato.
Mettendo insieme le nuove conoscenze di nutrigenetica, nutrigenomica e metagenomica si potrebbero però elaborare interventi individuali: la nutrizione personalizzata dovrà quindi tenere conto anche del tipo di microbiota della persona interessata.
È importante assumere alimenti ricchi di prebiotici che favoriscono la proliferazione dei batteri buoni nell’intestino come i bifidobatteri, quindi fibre e carboidrati complessi che si trovano nei cereali integrali, nella verdura e nella frutta. È importante assumere anche alimenti fermentati come lo yogurt e il kefir.
Non tutti i probiotici sono uguali, e favorirne la varietà nell’alimentazione è importante per aiutare a mantenere il microbiota in equilibrio. I probiotici si trovano in yogurt, in cibi fermentati (kefir, tempeh, crauti) e in tutti i cibi ricchi di fibre come le verdure e la frutta.
Alimenti che fanno bene al microbiota sono: orzo, miglio, farro, lenticchie, fagioli e piselli sono tutti fornitori di fibre e beta-glucani, importantissimi per il sostentamento del microbiota.
La rifaximina, principio attivo del NORMIX ® è un antibiotico appartenente alla famiglia delle rifamicine, particolarmente indicato nel trattamento delle infezioni microbiche intestinali, visto il suo scarso assorbimento sistemico, stimato al massimo intorno all’1%.
La possibilità di utilizzare l’analisi del microbiota, ovvero la composizione del microbiota intestinale, per prevedere, diagnosticare, seguire l’andamento di malattie metaboliche come obesità, resistenza insulinica o diabete di tipo due (T2D), da aggiungere ai convenzionali e validati, “classici” biomarcatori, richiede molta cautela anche da parte di personale esperto e qualificato.






