Composizione del microbiota e phyla batterici principali
|
Getting your Trinity Audio player ready...
|
Il microbiota è costituito da un elevato numero di cellule batteriche (circa 1 Kg di microrganismi) e da un elevato numero di specie batteriche (oltre 2.000 specie batteriche). I calcoli iniziali ritenevano che se il corpo umano è costituito in media da circa 1013 (10.000.000.000.000 o circa dieci trilioni) di cellule, i microorganismi che risiedono nel corpo umano adulto erano stimati intorno a 1014 cellule (100 trilioni ovvero 1.000.000 di miliardi), il che equivaleva a dire che il 90% del nostro corpo non è umano [Wu GD & Lewis JD, 2013]. Oggi invece si sa che il numero di batteri e cellule che compongono l’organismo umano è circa equivalente [Sender R, Fuchs S, Milo R, 2016], per cui risulta errato il rapporto almeno di 10:1 a favore dei batteri calcolato nel passato [Luckey T, 1972]: un uomo medio (considerando come riferimento una persona che pesa 70 chili, di 20-30 anni e alta 1,70 metri) contiene circa 30mila miliardi di cellule e 39mila miliardi di batteri.
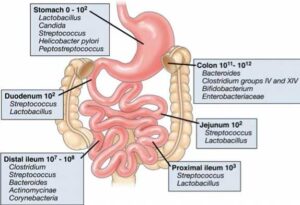 La composizione del microbiota è specifica di ogni individuo, deriva da una serie enorme di fattori, ha una differente distribuzione a seconda del tratto gastrointestinale interessato, con una variabilità intra e interpersonale, e cambia nel corso della nostra vita. Il normale rapporto simbiotico tra organismo umano e microbi è in funzione dell’omeostasi tra le due parti, in ragione soprattutto della diversità dei germi e della loro stabilità. Sicché il microbiota si adatta all’ospite, alla disponibilità delle risorse alimentari, all’ambiente, alle stagioni, allo stile di vita, alla società, all’esercizio fisico, etc.
La composizione del microbiota è specifica di ogni individuo, deriva da una serie enorme di fattori, ha una differente distribuzione a seconda del tratto gastrointestinale interessato, con una variabilità intra e interpersonale, e cambia nel corso della nostra vita. Il normale rapporto simbiotico tra organismo umano e microbi è in funzione dell’omeostasi tra le due parti, in ragione soprattutto della diversità dei germi e della loro stabilità. Sicché il microbiota si adatta all’ospite, alla disponibilità delle risorse alimentari, all’ambiente, alle stagioni, allo stile di vita, alla società, all’esercizio fisico, etc.
Delle diverse specie di microorganismi che popolano l’organismo umano, i più numerosi sono batteri, ma anche in misura inferiore miceti e virus. Tra i batteri la maggioranza è anaerobia, più o meno stretta o facoltativa (molti sopravvivono in assenza di ossigeno e alcuni ne tollerano la presenza). Il batterio intestinale più conosciuto nell’Uomo è l’Escherichia coli.
Va tuttavia precisato che, oltre alle cellule batteriche in rapporto simbiontico (ovvero sia l’ospite che i batteri traggono beneficio dalla co-presenza), esiste una piccola percentuale di batteri che vivono nell’organismo, ma non arrecano alcun beneficio ad esso (e quindi traggono solo un vantaggio per se stessi); nel sito in cui sono collocati non creano danno ma se cambiano habitat, come conseguenza di un trauma, possono determinare patologie anche gravi (esempio: Staphylococcus aureus ed endocarditi).
Il Regno Bacteria
Il regno Bacteria, dei batteri (sing. batterio) o eubatteri, comprende microrganismi unicellulari, procarioti, in precedenza chiamati anche schizomiceti, di dimensioni solitamente dell’ordine di pochi micrometri, ma che possono variare da circa 0,2 µm dei micoplasmi fino a 30 µm di alcune spirochete.
I microrganismi si classificano in “regni”, “phyla” e “classi”. Ad oggi, nell’insieme, sono stati individuati nel microbiota cinquanta phyla di batteri e 35.000 specie.
Il regno Bacteria comprende 30 phyla/divisioni: Acidobacteria, Actinobacteria, Aquificae, Armatimonadetes, Bacteroidetes, Caldiserica, Chlamydiae, Chlorobi, Chloroflexi, Chrysiogenetes, Cyanobacteria, Deferribacteres, Deinococcus, Dictyoglomi, Elusimicrobia, Fibrobacteres, Firmicutes, Fusobacteria, Gemmatimonadetes, Lentisphaerae, Nitrospira, Planctomycetes, Proteobacteria, Spirochaetes, Synergistetes, Tenericutes, Thermodesulfobacteria Thermomicrobia, Thermotogae, Verrucomicrobia.
Ogni phylum comprende numerose classi.
Albero filogenetico che descrive le relazioni evolutive tra gli esseri viventi. Tutti gli organismi appartengono a uno dei tre domini Bacteria, Archaea e Eucarya. I primi due costituiscono il gruppo dei procarioti e condividono con gli eucarioti l’origine da un progenitore comune a partire dal quale si sono differenziate le tre principali linee evolutive che hanno dato origine alle forme di vita conosciute.
Le cellule batteriche che compongono il microbiota possono anche raggrupparsi in due grandi ordini:
- I batteri autoctoni, sin dalla nascita nonché dopo lo svezzamento diventano colonie stabili permanenti con caratteristiche così particolari di alcuni ceppi tali da costituire per qualità e quantità un imprinting costante d’identificazione più preciso delle impronte digitali;
- I batteri alloctoni transitori, introdotti con il cibo, come formaggi, salumi e alimenti fermentati, che in caso di aumento eccessivo causano squilibri anche gravi dalla disbiosi alle malattie.
Nel microbiota residente vengono distinti batteri utili (soprattutto: Lactobacillus Acidophilus, Lactobacillus Bulgaricus e Bifidobatteri), dannosi (Acinetobacter baumannii. …
Pseudomonas aeruginosa. … Enterobacteriaceae. … Enterococcus faecium. … Staphylococcus aureus. …Helicobacter pylori. … Campylobacter. … Salmonella…) indifferenti.
Solo dopo lo svezzamento del bambino si ha la transizione della flora batterica verso il profilo dell’adulto.
Il microbiota colonizza virtualmente ogni superficie dell’organismo umano in qualche modo in contatto con l’ambiente esterno: pelle, vie urinarie, intestino e vie aeree.
Nella pelle, ad esempio, è distribuito, non solo negli strati più esterni, ma anche in quelli più profondi. L’apparato di gran lunga più ampiamente colonizzato è il tubo digerente o canale alimentare. Si stima che il colon da solo contenga più del 70% dei microbi presenti nell’organismo.
La maggior parte del microbiota intestinale è composta da microrganismi definiti anaerobi obbligati perché vivono esclusivamente in ambienti privi di ossigeno. Il loro numero è doppio o triplo rispetto agli anaerobi facoltativi (che vivono con e senza ossigeno) e gli aerobi (che vivono in presenza di ossigeno).
Le colonie più numerose sono delle specie Bacteriodetes e Firmicutes. Actinobacteria, Fusobacteria, Proteobacteria, Verrucomicrobia e altre sono presenti in minori quantità.
Occorre tuttavia precisare che, nonostante gli ampi studi condotti finora, ancora non è stato possibile identificare le singole specie che compongono il microbiota umano e quali ruoli svolgono nella salute umana. Questo perché molte specie sono poco abbondanti e altre non riescono a sopravvivere al di fuori dell’intestino. Significativo al riguardo un lavoro pubblicato su Nature [Almeida et al., 2019] grazie al quale è stato possibile superare questo problema utilizzando un software che ha analizzato le informazioni relative al DNA dei batteri gastrointestinali contenute nei database pubblici. Questo ha permesso di ricostruire le sequenze genetiche e di identificare circa 1.952 specie non conosciute prima.
Phyla batterici principali presenti nel microbiota intestinale
Il corpo umano, a eccezione di cervello e sistema circolatorio, ospita miliardi di microrganismi di circa 1.000 specie microbiche diverse.
I phyla batterici, ovvero le specie microbiche più rappresentate sono:
- Firmicutes (30-50%), tra cui Clostridium coccoides e leptum, Enterococcus, Faecalibacterium praunizii, Lactobacilli, Streptococcus thermophilus;
- Bacterioides (20-35%), tra cui i Bacteroides thetaiotaomicron;
- Actinobacteria (5%), come il Bifidobacterium; Verrucomicrobia (1%), tra cui l’Akkermansia;
- Proteobacteria (8-10%), come Escherichia coli ed Helicobacter.
- Cyanobacteria
Il microbioma è considerato la parte variabile del nostro genoma, in grado di adattarsi all’ambiente esterno. Il microbiota, infatti, si è modificato e si modifica nel corso dell’evoluzione in simbiosi con l’ospite, permettendo all’uomo di adattarsi alle varie condizioni di vita.
- Firmicutes
I Firmicutes costituiscono uno dei phyla più abbondanti assieme ai Bacteridetes e svolgono un ruolo significativo nella relazione fra i batteri intestinali e la salute dell’uomo. Molti membri di questo phylum scompongono i carboidrati che non possono essere digeriti nell’intestino dagli enzimi del corpo, come fibre dietetiche e gli amidi resistenti.
Il termine Firmicutes deriva dal latino firmus (forte) e cutis (pelle); i batteri sono caratterizzati da uno strato di peptidoglicano che conferisce loro durezza.
Sono batteri Gram+, comprendenti 250 generi suddivisi in due classi:
- Bacilli
- Clostridi
All’ordine Bacillales appartengono batteri aerobi facolativi o obbligati con la tipica forma a bastoncello; comprendono diverse famiglie: Bacillaceae, Lactobacillaceae, Leuconostocaceae, Streptococcaceae.
I Clostridia sono anaerobi obbligati che metabolizzano carboidrati e proteine con produzione di alcoli, acido acetico, acido butirrico e sostanze volatili come anidride carbonica, idrogeno e acido solfidrico. Circa l’8% degli adulti sono portatori sani di Clostridium difficile, che può causare diarrea, febbre, con sviluppo di colite pseudomembranosa in soggetti che assumono antibiotici.
La maggioranza dei Firmicutes rilevati nel tratto gastroenterico appartiene a due gruppi: il gruppo di Clostridium coccoides e il gruppo di Clostridium leptum.
Al gruppo di C. coccoides appartengono membri del genere Clostridium, Coprococcus, Dorea, Eubacterium, Lachnospira, Roseburia, Ruminococcus e Butyrivibrio. Gruppo predominante nel tratto gastroenterico (11-43% della popolazione microbica). Le specie di questo gruppo sono le maggiori produttrici di butirrato, fonte di energia per i colonociti.
Ma all’interno di questo phylum ci sono alcune specie patogene, come Clostridium perfringens e Clostridium difficile (tipi di batteri che causano infezioni gastrointestinali), Staphylococcus aureus che è causa comune di alcune infezioni gravi e altri batteri opportunistici gram-positivi.
Il Gruppo dei C. leptum comprende membri del genere Clostridium, Eubacterium, Ruminococcus e Anaerofilum. Sono anaerobi estremofili e anch’essi forti produttori di butirrato. Il più rappresentato è il Faecalibacterium prausnitzii (64%) sempre forte produttore di butirrato.
Eubatteri (bacilli Gram+) appartenenti alla normale flora intestinale sono E. contortum, E. nitritogenes, E. plautii, E. ramulus, E. ventriosum. I maggiori prodotti della fermentazione dei carboidrati sono acido butirrico, acetico e formico.
I Firmicutes e il phylum dei Proteobacteriae producono anche batteri solforiduttori. Metabolizzando composti contenenti zolfo come mucine e amminoacidi, questo gruppo produce l’acido solfidrico (H2S), considerato altamente tossico al di fuori di una gamma fisiologica strettamente regolata. Il phylum è coinvolto in molti processi metabolici, enzimatici e ormonali e nell’assorbimento di minerali, e il suo equilibrio è considerato cruciale per il benessere dell’intestino e degli altri organi.
La maggior parte dei probiotici immessi nel mercato appartiene alla famiglia delle Lactobaciliaceae, in particolare al genere Lactobacillus.
- Lactobacillaceae
Il genere Lactobacillus comprende numerose specie di batteri Gram + anaerobi facoltativi o microaerofili di forma bastoncellare.
In natura ne esistono almeno 60 specie e costituiscono la maggior parte del gruppo di batteri lattici, in quanto la quasi totalità dei loro membri converte il lattosio e altri zuccheri in acido lattico mediante la fermentazione lattica. Sono molto comuni e di solito non patogeni.
Negli esseri umani sono presenti nella vagina e nel tratto gastrointestinale, in cui sono simbiotici e costituiscono una piccola parte del microbiota umano.
I lactobacilli producono soprattutto acido lattico per fermentazione degli zuccheri, riducendo il pH dell’ambiente in cui crescono, ma anche acido acetico, etanolo, anidride carbonica ed altri composti secondari. L’acidificazione del loro ambiente (tenuto tra 3,5 e 4,5 di pH) inibisce la crescita di alcuni microrganismi patogeni.
Questa funzione ha riscontro nella vagina, dove il Lactobacillus costituisce il 97%-98% della flora microbica normale ed evita la proliferazione di altri microbi lasciando il pH su valori attorno al 5. I lactobacilli sono distinti in
- omofermentativi, nel caso producano quasi esclusivamente acido lattico, oppure
- eterofermentativi, se producono anche altri composti come l’acido acetico.
Nella vagina si ritrovano varie specie di cui la più abbondante è L. acidophilus, in minor misura L. brevis, L. casei, L. crispatus, L. fermentum, L. jensenii, L. plantarum, tutti denominati con il termine di «bacillo di Döderlein».
Cavità orale: L. casei, L. fermentum.
Intestino: L. acidophilus, L. bifidus, L. catenaformis, L. brevis, L. casei, L. delbrueckii, L. crispatus (nelle feci), L. fermentum, L. gasseri, L. plantarum, L. salivarius.
Al gruppo dei batteri produttori di acido lattico (LAB), come prodotto finale della fermentazione e dei processi metabolici, appartengono altri batteri quali Lactococcus, Enterococcus, Streptococcus e Leuconostoc.
- Streptococchi
Gli Streptococchi intestinali, isolati nelle feci e dalla cavità orale, possono causare vari processi patologici nell’uomo:
- acidominimus (a-emolitico, produce piccolissime quantità di acido dalla fermentazione dei carboidrati), gruppo degli streptococchi vari.
- anginosus (a-emolitico), streptococco orale
- bovis (gruppo D, a-emolitico), streptococco fecale.
- intermedius (a-emolitico o non emolitico), streptococco orale.
- milleri (a-emolitico, b-emolitico o non emolitico), streptococco orale.
- mitis (a-emolitico), streptococco orale.
- mutans (a-emolitico o non emolitico), streptococco orale.
- pleomorphus (a-emolitico), gruppo degli streptococchi anaerobi.
- salivarius (a-emolitico o non emolitico), streptococco orale.
- sanguinis (a-emolitico, raramente b-emolitico o non emolitico), streptococco orale.
Bacteroidetes
ll phylum Bacteroidetes comprende tre classi:
- Bacteriales
- Sphingobacteriales
- Flavobacteriales.
Nella classe Bacteriales il genere Bacteroides costituisce il 24-25% del microbiota GI.
Sono specie anaerobiche Gram-, con struttura a bastoncino, non formanti spore e resistenti ai sali biliari, con notevoli capacità adattative. Dalla fermentazione dei carboidrati viene prodotta una miscela di vari acidi organici: succinico, acetico, lattico, formico, propionico; raramente viene prodotto acido butirrico.
Sono stati ritrovati nelle feci umane e nel microbiota intestinale: B. distasonis, B. coagulans, B. fragilis, B. eggerthii, B. galacturonicus, B. merdae, B. pectinophilus, B. putredinis, B. stercoris, B. ureolyticus etc….
I Bacteroides
- giocano un ruolo importante nel degradare molecole complesse in forme semplici per l’intestino dell’ospite;
- possono utilizzare semplici zuccheri come fonte energetica, ma se questi non sono disponibili possono utilizzare i glicani derivanti dalle piante;
- sono associati a diete ricche di proteine animali a grassi saturi, mentre specie batteriche come la Prevotella aumentano nel microbiota intestinale quando l’ospite ha una dieta ricca di carboidrati e zuccheri semplici;
La specie più importante dal punto di vista clinico è il Bacteriodes fragilis che può trasformarsi in patogeno opportunistico e causare appendicite ed infezioni nella cavità peritoneale.
In generale, Bacteroides sono resistenti agli antibiotici β-lattamici, aminoglicosidici ma sensibili a metronidazolo e cloramfenicolo.
Uno squilibrio dei Bacteroidetes sembra essere correlato a: obesità, malattie infiammatorie intestinali come il morbo di Crohn e la colite ulcerosa.
Proteobacteria
A questo phylum appartiene la famiglia delle Enterobacteriaceae, che include un numero ampio di batteri, come Escherichia coli, Salmonella typhi, Vibrio cholerae, Helicobacter pylori, etc. il cui habitat naturale è costituito dall’intestino dell’uomo e di altri animali. Questi batteri sono accomunati da caratteristiche antigeniche e biochimiche tipiche dell’intero gruppo.
Tutti gli Enterobatteri sono bastoncelli Gram-negativi, asporigeni. Possono essere mobili o immobili, quasi tutti provvisti di pili. Sono aerobi-anaerobi facoltativi e normali terreni di coltura consentono la loro crescita. La superficie della cellula degli enterobatteri vede la presenza di molecole di lipopolisaccaride (LPS), caratteristica comune di tutti i batteri Gram-negativi. Questa molecola contribuisce alla proprietà tossica di questi batteri.
Questo gruppo di batteri è coinvolto in molti processi di riduzione dei nitrati e denitrificazione, grazie alle attività di nitrati periplasmatici reduttasi (Nap), nitrito reduttasi contenenti rame (Cu-Nir), citocromo c ossidasi NO reduttasi (cNor) e ossido nitroso reduttasi (Nos). Lo squilibrio di questo phylum viene considerato particolarmente importante in molte malattie.
Gli enterobatteri sono responsabili di varie manifestazioni infettive:
- Infezioni sistemiche, causate dalle febbri enteriche, quali tifo e paratifo.
- Infezioni intestinali, costituite da gastroenteriti o enteriti causate da batteri di stipiti specifici del genere Escherichia, Salmonella e Shigella. I sintomi sono diarroici e dissenterici.
- Infezioni urinarie, quasi sempre causate da alcuni tipi di Escherichia coli.
Actinobacteria
Gli Actinobacteria includono per la maggior parte batteri Gram-positivi come: coccoide (Micrococcus), bacilliforme (Arthrobacter), frammenti di ifa (Nocardia spp.), micelio (Streptomyces spp). Questi batteri possiedono diverse proprietà fisiologiche e metaboliche come la produzione di enzimi e formazione di vari metaboliti.
La stragrande maggioranza di Actinobacteria sono importanti saprofiti capaci di scomporre un’ampia gamma di rifiuti vegetali e animali nel processo di scomposizione. Questo phylum include i gruppi Streptomyces e Micromonospora, riconosciuti come produttori di molti metaboliti bioattivi utili all’uomo in qualità di antimicrobici, inibitori di enzimi e sostanze di controllo dell’equilibrio intestinale (molecole di segnalazione e immunomodulatori).
Il phylum include anche patogeni (Mycobacterium spp., Nocardia spp., Tropheryma spp., Corynebacterium spp. e Propionibacterium spp.), abitanti del suolo (Streptomyces spp.), commensali delle piante (Leifsonia spp.), simbioti fissanti l’azoto (Frankia), ed abitanti del tratto gastrointestinale (Bifidobacterium spp.).
Le Bifidobacteriaceae comprendono 4 generi, Bifidobacterium, Gardnerella, Scardovia, e Parascardovia. Il genere Bifidobacterium contiene 6 specie: B. boum, B. asteroides, B. adolescentis, B. longum, B. pullorum, e B. pseudolongum.
I Bifidobacteria sono anaerobi, non mobili, non sporulano, non producono gas. Sono stati isolati in diverse nicchie ecologiche: intestino, cavità orale, cibi. La lista degli effetti positivi dei Bifidobacteria (che includono almeno 100 specie diverse) è molto lunga: regolazione dell’omeostasi microbica intestinale, inibizione di batteri opportunistici e dannosi, modulazione di risposte immunitarie, repressione di composti cancerogeni, produzione di vitamine, bioconversione di composti dietetici in molecole bioattive, riduzione di endotossine LPS nell’intestino. Sono inoltre coinvolti nel miglioramento della riduzione della colite ulcerosa e nella gestione dietetica dei FODMAP nella Sindrome del colon irritabile (IBS).
- Vedi sotto: Bifidobatteri
- Cyanobacteria
I Cyanobacteria sono batteri gram-negativi che includono cinque tipi di produttori di tossine e altri batteri utili ben noti per le loro importanti caratteristiche fototropiche a livello ecologico. Si distinguono per la loro abilità di eseguire la fotosintesi ossigenica (fotosintesi vegetale, evolvente in ossigeno e con ossidazione dell’acqua).
I Cyanobacteria, insieme al gruppo dei Melainabacteria, provvedono alla sintesi di diverse vitamine B e K nell’intestino umano; ciò suggerisce che questi batteri siano benefici per l’ospite poiché possono agevolare la digestione delle fibre vegetali.
- Acinetobacter
Il genere Acinetobacter è un coccobacillo ubiquitario gram-negativo non mobile. Molte specie di Acinetobacter ricordano le pseudomonadi saprofite e altri organismi gram-negativi non fermentativi per quanto riguarda la loro abilità di utilizzare un’ampia gamma di composti organici come unica fonte di carbonio ed energia. La colonizzazione rettale di Acinetobacter comporta il rischio del fenomeno di “traslocazione” (il trasferimento dall’intestino a siti di infezione situati nei polmoni o in altri organi).
L’Acinetobacter spp. è opportunistico in ambienti di cura ospedalieri e domiciliari. Il tasso di colonizzazione di Acinetobacter spp. nella pelle, nella mucosa orale e nel tratto gastrointestinale aumenta rapidamente dopo un ricovero ospedaliero e in particolare all’interno di un reparto di terapia intensiva (ICU).
- Clostridium
Il genere Clostridium è un gruppo di batteri gram-positivi strettamente anaerobi che hanno l’abilità di produrre un particolare tipo di cellula dormiente: l’endospora. Sono state scoperte circa 100 specie di Clostridium, e alcune di esse sono responsabili di malattie umane causate dalla formazione di tossine.
La loro presenza eccessiva nel tratto intestinale è considerata un esito negativo; soltanto i grappoli Clostridium XIVa e IV possiedono alcuni attributi benefici (sono particolarmente bassi nei pazienti che soffrono di malattie infiammatorie intestinali, o IBD). La presenza di Clostridium difficile nell’intestino potrebbe causare la produzione di diverse tossine come quelle citotossiche (tipo A e B).
- Turicibacter
Il genere Turicibacter appartiene al phylum dei Firmicutes e si trova generalmente nell’intestino. Il suo ruolo è controverso. È coinvolto nel metabolismo dei lipidi e degli steroidi dell’ospite. La sua presenza eccessiva è inversamente correlata all’esercizio, al morbo di Crohn, al metabolismo della serotonina/triptofano, ma non nelle malattie autoimmuni.
È nota solamente una specie formante spore, la Turicibacter sanguinis. La presenza di Turicibacter nell’intestino è importante quando è abbondante ma non eccessiva.
- Haemophilus
Il genere Haemophilus è un batterio bastoncellare molto piccolo appartenente alle Pasteurellaceae (Proteobacteria). Tutte le specie di Haemophilus sono patogeni strettamente opportunistici presenti nel tratto respiratorio degli animali a sangue caldo fra cui gli esseri umani, nonché in alcuni animali a sangue freddo.
Anche se il tasso di presenza di batteri Haemophilus nel microbiota intestinale è ancora sconosciuto, la sua presenza in quantità abbondanti è stata correlata di recente a schizofrenia/depressione e ad altri effetti infiammatori gravi (es. gastroenterite, peritonite).
- Helicobacter
I membri del genere Helicobacter (Proteobacteria phylum) colonizzano lo stomaco (specie gastrica), fegato (specie enteroepatica) e l’intestino. Il rilascio di ureasi da parte delle specie gastriche di Helicobacter come l’H. pylori, genera ammoniaca per neutralizzare la nicchia dello strato mucoso gastrico portando il pH a 6-7, ed è considerato un meccanismo di sopravvivenza.
L’Helicobacter causa malattie diarroiche ed è associato all’ulcera peptica, e viene considerato inoltre come un fattore di rischio per il cancro gastrico. L’Helicobacter è parte del tratto gastrointestinale, e qualora presente in elevata quantità può produrre adesine, enzimi citotossici ed enterotossine di natura infiammatoria.
- Klebsiella
Il genere Klebsiella è un genere di batterio bastoncellare dritto gram-negativo anaerobico facoltativo non formante spore e non mobile, appartenente al phylum dei Proteobacteria. I microrganismi Klebsiella generalmente sono presenti nell’ambiente, ma possono anche colonizzare in maniera asintomatica il tratto rinofaringeo e quello gastrointestinale e, meno frequentemente, altri siti.
Un’alta colonizzazione gastrointestinale di Klebsiella può preannunciare un’infezione addominale, aumentando il rischio di infezione addominale di ben sette volte, così come il tasso di colonizzazione nei pazienti ospedalizzati. Il genere Klebsiella come batterio fermentativo può metabolizzare il glucosio con la produzione di acido e di gas.
- Escherichia
Il genere Escherichia appartiene alla famiglia delle Enterobacteriaceae (phylum Proteobacteria), un gruppo di bacilli gram-negativi responsabili di una vasta gamma di infezioni in esseri umani e animali. Dalla fermentazione dei carboidrati derivano sia acido che gas. Soltanto alcuni zuccheri come l’inositolo non vengono utilizzati, e il ribitolo viene utilizzato solo da una specie.
Il lattosio viene fermentato rapidamente da molti membri, producendo grandi quantità di acidi e gas. Come molte Enterobacteriaceae, l’Escherichia può influenzare lo stato infiammatorio tramite l’alto numero di LPS (tossina lipopolisaccaride) presente sulla membrana esterna e sulle pareti cellulari.
- Prevotella
Il genere Prevotella (phylum Bacteroidetes) include bastoncellari gram-negativi comunemente associati alla colonizzazione della bocca e dell’intestino umani. Questo genere ha l’abilità di idrolizzare xilani e pectine e di utilizzare i prodotti della decomposizione derivanti dalla degradazione delle pareti cellulari vegetali. Si ritiene che questo genere abbia un ruolo importante nel metabolismo delle proteine e dei peptidi, poiché molti ceppi sono attivamente proteolitici e possiedono una caratteristica attività di dipeptidil-peptidasi.
Le specie Prevotella sono coinvolte nella sinusite cronica, infezioni dell’orecchio medio, ascessi cerebrali, ascessi intra-addominali, e di recente sono state correlate ad alcune malattie autoimmuni. I meccanismi virulenti includono un attaccamento alla mucosa, evasione immunitaria, produzione di proteasi e un’eccessiva produzione di fattori virulenti quando si verifica la transizione del microrganismo da commensale a patogeno.
- Salmonella
Il genere Salmonella include più specie di anaerobi facoltativi. Sono catalasi positivi, ossidasi negativi e fermentanti glucosio, mannitolo e sorbitolo con la produzione di acidi o acidi e gas. Solo S. arizonae è in grado di fermentare il lattosio, e ciò rappresenta un’eccezione piuttosto che una regola. Il gruppo Salmonella è in grado di fermentare il saccarosio, più raramente il ribitolo, e generalmente non forma indolo. Formano un gruppo centrale nella famiglia delle Enterobacteriaceae e sono considerate una causa fondamentale delle malattie di origine alimentare negli esseri umani e una causa significativa di morbilità, mortalità e perdita economica a livello globale.
Alcuni sierotipi (oggi ce ne sono più di 2.500) possono colonizzare regolarmente l’intestino. Le malattie vanno dalla gastrointerite lieve a quella grave, e in alcuni soggetti la malattia invasiva può essere fatale. Le complicazioni a lungo termine come l’artrite reattiva e la sindrome del colon irritabile sono state individuate come esito negativo e come conseguenze della salmonellosi.
- Streptococcus
Il genere Streptococcus appartiene alla famiglia delle Micrococcaceae (phylum Firmicutes), e consiste in 104 specie riconosciute, sia commensali che patogene. Le specie di Streptococci possono essere definite utilizzando lo schema di classificazione di Lancefield, un tipo di classificazione sierotipica. Lo Streptococcus di gruppo A (GAS) include lo Streptococcus pyogenes: si stima che lo Streptococcus di gruppo A sia causa di 240.000 malattie di origine alimentare all’anno.
Anche altri gruppi di Streptococcus sono stati occasionalmente rilevati in malattie di origine alimentare. I sintomi della malattia sono molto diversi dalla maggioranza delle malattie di origine alimentare, dal momento che la malattia non include la gastrointerite ma più comunemente una gola infiammata; le complicazioni includono febbre reumatica acuta e infiammazione renale. Lo Streptococcus viene considerato un agente infiammatorio che causa anche setticemia, endocardite, polmonite e molte infezioni dei tessuti.
- Sutterella
Il genere Sutterella è un genere di batteri anaerobi gram-negativi non formanti spore appartenente alla famiglia Sutterellaceae (Phylum Proteobacteria). I membri del genere Sutterella sono per la gran parte commensali con lieve capacità proinfiammatoria nel tratto gastrointestinale umano. Tuttavia, l’aumento di Sutterella è correlato a diversi disordini della flora intestinale e alle infiammazioni intestinali.
La Sutterella è inoltre correlata alla disbiosi intestinale e a disordini neurologici come autismo, sindrome di Down o altre malattie autoimmuni e infiammatorie come le IBD (malattie infiammatorie intestinali). L’iper-produzione di LPS (lipopolisaccaridi) dovuta all’aumento del genere Sutterella nell’intestino può essere considerata il fattore patogeno principale delle proprietà infiammatorie.
- Alistipes
Il genere Alistipes è un genere relativamente nuovo di batteri isolati principalmente nei campioni clinici. Nonostante sia presente in percentuale minore rispetto ad altri membri del genere del phylum Bacteroidetes nell’intestino, la sua presenza in grande quantità è considerata rilevante nella disbiosi e nelle malattie intestinali. Secondo la banca dati di tassonomia del National Center for Biotechnology Information, il genere comprende 13 specie.
È stato dimostrato che tutte le specie di Alistipes producono sulfonolipidi, che si pensa abbiano capacità infiammatorie. Il genere Alistipes ha delle implicazioni emergenti in molti processi infiammatori, nel cancro al colon e nella salute mentale. La disbiosi intestinale con un alto numero di Alistipes nelle feci sembra avere un ruolo anche in altre malattie del metabolismo, come nella steatoepatite non alcolica, encefalopatia epatica e fibrosi epatica.
Batteri proinfiammatori e antinfiammatori rinvenuti nel microbiota intestinale
| Batteri proinfiammatori | Batteri antinfiammatori |
| · Acinetobacter | · Akkermansia |
| · Clostridium | · Bifidobacterium |
| · Turicibacter | · Enterococcus |
| · Haemophilus | · Eubacterium |
| · Helicobacter | · Faecalibacterium |
| · Klebsiella | · Lactobacillus |
| · Escherichia | · Oxalobacter |
| · Prevotella | · Parabacteroides |
| · Salmonella | · Ruminococcus |
| · Streptococcus | · Coprococcus |
| · Sutterella | |
| · Alistipes |
- Akkermansia
Akkermansia è un genere di microbi intestinali umani con un ruolo di primo piano nella fisiologia dello strato di muco intestinale ed è associato alla diminuzione della massa corporea e all’aumento della funzione e della salute della barriera intestinale. La relativa abbondanza di A. muciniphila sembra inversamente correlata all’obesità negli esseri umani, ed è stato dimostrato che, nei topi con obesità indotta dalla dieta, allevia la resistenza all’insulina e l’obesità aumentando al tempo stesso la funzione di barriera intestinale.
Si pensa che questa attività sia secondaria ad un’alterazione della produzione microbica di acidi grassi a catena corta (SCFA). Questi studi supportano meccanismi, oltre alla perdita di peso, che migliorano le malattie metaboliche e infiammatorie.
- Bifidobacterium
I bifidobatteri sono considerati microrganismi probiotici che, in generale, sono utili per mantenere adeguati equilibri tra le varie flore in diverse sezioni dell’intestino umano. Alcuni ceppi di Bifidobacterium di origine umana sono in grado di sintetizzare determinate vitamine. Per esempio, tiamina, acido folico, biotina e acido nicotinico sono sintetizzati in quantità apprezzabili da B. bifidum e B. infantis, mentre B. breve e B. longum rilasciano solo piccole quantità di queste vitamine. Queste ultime specie sono produttrici riconosciute di riboflavina, piridossina, cobalamina e acido ascorbico.
Le note proprietà benefiche per la salute associate all’ingestione di Bifidobacterium spp. sono le seguenti: miglioramento della digestione del lattosio, aumento dei bifidobatteri fecali, riduzione dell’attività degli enzimi fecali, colonizzazione del tratto intestinale, prevenzione o cura della diarrea acuta causata da infezioni di origine alimentare, prevenzione o cura della diarrea da rotavirus, prevenzione della diarrea indotta da antibiotici, prevenzione o cura della sindrome dell’intestino irritabile (IBS) e di malattie infiammatorie intestinali (IBD). Gli altri benefici per la salute attribuiti ai bifidobatteri includono:
- attività contro Helicobacter pylori;
- stimolazione dell’immunità intestinale;
- stabilizzazione della peristalsi intestinale;
- tempo di trasporto ridotto per Salmonella spp.;
- miglioramento dell’immunità a varie malattie;
- soppressione di alcuni tumori;
- riduzione dei livelli sierici di colesterolo;
- riduzione dell’ipertensione.
I membri del genere Bifidobacterium sono tra i primi microbi a colonizzare il tratto gastrointestinale umano e dominano la popolazione batterica intestinale totale nei neonati sani allattati al seno, sebbene questa predominanza diminuisca dopo lo svezzamento. Nel corso della vita adulta, infatti, la popolazione dei bifidobatteri inizia a diminuire, mentre negli anziani spesso si riduce drasticamente fino a scomparire.
- Enterococcus
Gli enterococchi sono un antico genere di batteri dell’acido lattico (LAB) altamente adattati a vivere in ambienti complessi e a sopravvivere a condizioni avverse. Sono onnipresenti, abitano i tratti gastrointestinali di un’ampia varietà di animali, dagli insetti all’uomo. Questo modello diffuso di colonizzazione suggerisce che gli Enterococchi siano stati membri del microbioma intestinale di antichi antenati comuni.
I ceppi di enterococchi possono essere trovati in una varietà di alimenti fermentati, contribuiscono alla maturazione e allo sviluppo dell’aroma di alcuni formaggi o salsicce fermentate, nonché nei probiotici per migliorare la salute umana o animale. La crescita di alcuni ceppi di enterococchi, in particolare E. faecalis e E. faecium, è considerata altamente auspicabile e può svolgere un ruolo importante nel metabolizzare le sostanze nel cibo e nel latte attraverso la proteolisi, la lipolisi e la scomposizione del citrato. Tuttavia, alcuni Enterococchi portano potenziali fattori di virulenza e possono mostrare tratti patogeni.
- Eubacterium
Questo genere è costituito da specie filogeneticamente e – abbastanza di frequente – fenotipicamente diverse, che rendono l’Eubacterium un genere tassonomicamente unico e di difficile comprensione. La capacità di utilizzare il glucosio e gli intermedi di fermentazione del glicano acetato e lattato per formare butirrato o propionato è un punto chiave dell’Eubacterium all’interno delle interazioni trofiche, con il potenziale di avere un forte impatto sull’equilibrio metabolico con un impatto finale sul microbiota intestinale/omeostasi dell’ospite e sulla salute di quest’ultimo.
È infatti ben riconosciuto il suo importante ruolo nell’omeostasi energetica, nella motilità del colon, nell’immunomodulazione e nella soppressione dell’infiammazione nell’intestino. L’Eubacterium spp. esegue anche le trasformazioni degli acidi biliari e del colesterolo nell’intestino, contribuendo così alla loro omeostasi. La disbiosi intestinale e, di conseguenza, una rappresentazione modificata dell’Eubacterium spp. nell’intestino sono stati collegati a vari stati di malattia negli esseri umani.
- Faecalibacterium
Il Faecalibacterium prausnitzii è un batterio Gram-positivo, unico membro del genere Faecalibacterium, che costituisce dal 3% al 5% circa del microbiota fecale umano e può aumentare fino al 15% in alcuni individui. È stato costantemente indicato come uno dei principali produttori di butirrato presenti nell’intestino. Il butirrato ha un ruolo cruciale per la fisiologia intestinale e il benessere dell’ospite.
È la principale fonte di energia per i colonociti e ha proprietà protettive contro il cancro del colon-retto e le malattie infiammatorie intestinali. Un’abbondanza alterata di questo microbo è stata segnalata nelle malattie infiammatorie, come il morbo di Crohn, nonché nei disturbi depressivi, dimostrando il suo ruolo cruciale nella salute umana. Il cambiamento della composizione e della funzione del microbioma intestinale è riportato anche nelle malattie cardiovascolari, come l’insufficienza cardiaca cronica, in cui è stata recentemente dimostrata una diminuzione dell’abbondanza di Faecalibacterium prausnitzii.
- Lactobacillus
I batteri appartenenti al genere Lactobacillus sono membri dei batteri dell’acido lattico (LAB), un gruppo ampiamente definito caratterizzato dalla formazione di acido lattico come unico o principale prodotto finale del metabolismo dei carboidrati. Le specie commensali di Lactobacillus possono ripristinare l’omeostasi nei disturbi intestinali e, pertanto, svolgere un ruolo protettivo contro le malattie infiammatorie. In particolare, le specie di Lactobacillus presenti nell’intestino hanno ricevuto un’enorme attenzione per via delle loro proprietà benefiche per la salute. Sono comunemente usati come probiotici, definiti dalla FAO/OMS come microrganismi vivi che, se somministrati in quantità adeguate, comportano un beneficio per la salute dell’ospite. I probiotici che contengono Lactobacilli sono stati usati terapeuticamente per modulare l’immunità, abbassare il colesterolo, trattare l’artrite reumatoide, prevenire il cancro, migliorare l’intolleranza al lattosio e prevenire o ridurre gli effetti della dermatite atopica, del morbo di Crohn, della diarrea e della stitichezza, nonché della candidosi e delle infezioni del tratto urinario (UTI).
I probiotici Lactobacillus sono stati proposti anche come mezzi per potenziare le difese naturali dell’ospite ripristinando la presenza della normale microflora vaginale. Non tutti i probiotici sono uguali. I probiotici Lactobacillus devono avere la capacità di base di
- aderire alle cellule;
- escludere o ridurre l’aderenza patogena;
- persistere e moltiplicarsi;
- produrre acidi, perossido di idrogeno e batteriocine antagoniste della crescita dei patogeni;
- resistere ai microbicidi vaginali, compresi gli spermicidi;
- essere sicuri e quindi non invasivi, non cancerogeni e non patogeni; e
- coaggregarsi e formare una flora normale ed equilibrata.
- Oxalobacter
Oxalobacter è un genere di batteri anaerobici Gram-negativi che dipendono dal metabolismo dell’ossalato per produrre energia e che colonizzano l’intestino umano. L’O. formigenes svolge un ruolo essenziale nella regolazione del trasporto intestinale netto di ossalato. Si ritiene che la mancanza di O. formigenes nel colon aumenti l’assorbimento intestinale di ossalato, portando ad un aumento dell’escrezione di ossalato urinario, quindi aumentando la probabile incidenza della formazione di calcoli renali. Gli isolati umani di O. formigenes sono suscettibili a molti antibiotici comunemente usati. Di conseguenza, lo stato di colonizzazione potrebbe riflettere lo stato di salute, le abitudini alimentari o l’esposizione agli antibiotici.
Risorse per l’Oxalobacter possono essere latte crudo e yogurt, sottaceti, pomodori, cetrioli, spinaci e piante di dieffenbachia. È stato dimostrato che questo genere, insieme ad alcuni ceppi specifici di Lactobacilli e Bifidobacteria, ha la capacità di degradare l’ossalato presente nell’intestino e di far fronte ai calcoli renali.
- Parabacteroides
Parabacteroides è un genere relativamente nuovo con caratteristiche distintive condivise da altri batteri commensali intestinali. P. distasonis è il ceppo tipo di riferimento per il genere Parabacteroides, noto per il suo ipotetico contributo alla produzione locale di metano antinfiammatorio. Si ritiene che la fermentazione del P. distasonis porti alla produzione di metano. Non è chiaro se la produzione diretta di metano avvenga nel P. distasonis; tuttavia, è noto che il P. distasonis produce idrogeno, anidride carbonica, acido formico, acido acetico, acido carbossilico e acido succinico. Altri microbi possono convertire l’anidride carbonica e l’acido acetico in metano. I batteri acetogeni potrebbero quindi ossidare gli acidi, ottenendo più acido acetico e idrogeno o acido formico. Infine, nelle comunità intestinali complesse, i metanogeni possono convertire l’acido acetico in metano.
Gli studi suggeriscono che il P.distasonis potrebbe persino avere il potenziale per fungere da probiotico per promuovere la salute dell’apparato digerente nel microbioma umano. Tuttavia, altri dati sperimentali mostrano risultati contraddittori: ecco perché il P. distasonis potrebbe avere un ruolo dicotomico a seconda del contesto. Recentemente, è stato anche riportato che i pazienti con psoriasi hanno un microbiota intestinale con una minore abbondanza di Parabacteroides rispetto agli individui sani.
- Ruminococcus
Il genere Ruminococcus è definito come cocchi strettamente anaerobici, Gram-positivi, non mobili che non producono endospore e richiedono carboidrati fermentabili per la crescita. Si tratta di un gruppo di importanti mutualisti microbici intestinali, utili a degradare e convertire i polisaccaridi complessi in una varietà di nutrienti per i loro ospiti. Inoltre, questi batteri hanno sviluppato la capacità di decostruire e utilizzare un’ampia gamma di polisaccaridi vegetali con implicazioni per la salute dell’ospite. L’abbondanza di alcuni batteri commensali (Clostridium cluster XIVa e Clostridium cluster IV, che includono il Ruminococcus) è ridotta nei pazienti con IBD. Anche in questo caso, l’attività è correlata alla loro capacità di produrre butirrato. Pertanto, è stata accentuata l’importanza di una dieta arricchita di fibre per gli individui affetti da IBD, a causa della prevista modulazione della composizione del microbioma intestinale, inducendo un aumento dei batteri produttori di butirrato come il Ruminococcus.
Ruminococcus, Faecalibacterium, Eubacteria, Akkermansia, che producono butirrato e propionato, possono migliorare l’obesità negli individui (gli individui obesi hanno un aumento di batteri non produttori di butirrato come l’E. coli). I taxa produttori di butirrato sono anche ridotti nei soggetti con diabete mellito di tipo 2 (T2DM).
- Coprococcus
I geni del Coprococcus sono cocchi Gram-positivi anaerobici ospitati nell’intestino. Questo gruppo di batteri è anche associato al mantenimento e/o al miglioramento dell’omeostasi microbica nell’ospite mediante interazioni sinergiche con il microbiota endogeno benefico ed è noto per i suoi effetti antipatogeni, agendo per esclusione competitiva, aumento della funzione di barriera epiteliale e/o produzione di composti antimicrobici.
Il microbiota intestinale varia a seconda delle regioni anatomiche, anche perché in ogni tratto possono cambiare:
- fisiologia;
- valore del pH;
- tensione di ossigeno molecolare (O2);
- velocità del flusso digerente (che rallenta durante il percorso)
- disponibilità di substrato energetico;
- secrezioni intestinali.
L’intestino crasso, ad esempio, è caratterizzato da flussi lenti, pH tendente al neutro e ospita la maggior parte della comunità microbica. Infatti, procedendo lungo il tratto gastrointestinale vi è una riduzione nel numero di specie presenti ma un aumento quantitativo del microbiota: saranno presenti meno specie ma più specializzate e in unità nettamente superiore.
Dati preliminari
- Sindrome del colon irritabile (IBS)
In caso di Sindrome del colon irritabile (Irritable Bowel Syndrom o IBS) sono state osservate significative riduzioni nella concentrazione di batteri della specie Lactobacillus nei campioni fecali di pazienti con IBS rispetto ai controlli sani. Questa minore ricchezza microbica può portare ad una ridotta:
- sintesi di amminoacidi;
- integrità delle giunzioni cellulari;
- risposta infiammatoria.
Queste variazioni suggeriscono che vi sia una debolezza diffusa delle funzioni di barriera epiteliale, che spiega parzialmente i sintomi dell’IBS.
- Morbo celiaco
È stato riscontrato che la disbiosi è collegata a un ambiente infiammatorio nei pazienti celiaci. I pazienti mostrano, rispetto ai soggetti sani, una riduzione delle principali specie benefiche (Lactobacillus e Bifidobacterium) e un aumento di quelle potenzialmente patogene (Bacteroides ed E. coli). Questa può essere una chiave di lettura e di possibile intervento con terapie parallele per aiutare le persone a migliorare la qualità della loro vita.
- Implicazioni extra-intestinali
La relazione mutualistica microbiota-ospite sembra avere un ruolo centrale per molte malattie metaboliche e neurologiche.
Il microbiota, con tutto il suo microbioma, ha un impatto diretto sulla trasmissione nervosa dell’organismo. Esso influenza le nostre emozioni e il nostro comportamento: infatti, gli studi forniscono la prova che il microbioma interagisce con il sistema nervoso centrale.
Recenti studi hanno evidenziato che persone con un microbioma molto diversificato, tendono a costruire relazioni sociali più ampie. Viceversa stress e alterazioni dell’umore sono legati a una ridotta diversità e alterata composizione del microbiota.
È stato osservato in studi con soggetti sani che dopo tre settimane di somministrazione di prebiotici i livelli di cortisolo, comunemente detto “l’ormone dello stress”, erano diminuiti. In altri studi con pazienti con IBS, dopo un mese di integrazione prebiotica, si evidenziava una riduzione dell’ansia.
Recentissimi studi hanno mostrato che la depressione dovuta a eventi di vita stressanti cronici è associata ad un aumento di Enterobacteriaceae, mentre lo stress psicologico è associato a una riduzione di Lactobacilli spp. e un aumento di Escherichia coli e Pseudomonas spp.
Altri fattori che influenzano il microbiota
- Azione degli antibiotici
La somministrazione di antibiotici influenza il microbiota intestinale: essi ne modificano la composizione, incidono nell’abbondanza, diminuzione o scomparsa di alcune specie. L’alterazione della composizione del microbioma dipende diversi fattori: dal tipo di antibiotico, dal periodo di esposizione, dall’azione farmacologica.
Lo stato fisiologico dell’organismo e la composizione del microbiota prima della somministrazione dell’antibiotico inciderà sulla composizione microbiotica a termine del trattamento.
- Microbiota e indice di massa corporea (BMI)
L’Indice di Massa Corporea (Body Mass Index o BMI) è un parametro che fornisce una stima dello stato generale del peso forma. Pur non essendo un indice preciso, in quanto prende in considerazione solo peso corporeo e altezza, può essere utile come parametro di riferimento. Studi hanno evidenziato che alterazioni del microbiota sono strettamente in relazione con fattori legati all’obesità; inoltre ristabilire un microbiota efficiente può avere potenziali implicazioni terapeutiche.
I livelli di BMI possono essere utilizzati come valore predittivo per valutare la disbiosi del microbiota intestinale. Infatti, studi hanno dimostrato che un deperimento del microbiota è correlato all’esaurimento della produzione di Acidi Grassi a Catena Corta (Short Chain Fatty Acids o SCFAs): questo fattore può contribuire alla fisiopatologia dell’obesità. Inoltre è stato osservato che i bambini con BMI normale hanno una maggiore diversità microbica rispetto ai bambini sottopeso.
- Microbiota e attività motoria
È stata studiata anche l’associazione tra la frequenza di esercizio fisico con la composizione del microbiota intestinale in bambini piccoli e adolescenti: è stato riscontrato che l’esercizio quotidiano aumenta la diversità microbica intestinale.
Una maggiore diversità può anche produrre quantitativi maggiori di SCFAs: essi possono aumentare l’espressione di proteine a giunzione stretta negli epiteli del colon per aumentare la resistenza della barriera intestinale. Questa resistenza permette di ridurre la permeabilità della mucosa e di inibire le citochine pro-infiammatorie.
Inoltre un po’ di attività fisica, oltre a migliorare il tono muscolare, migliora anche l’umore aiutando a ridurre lo stress e i suoi effetti sull’intestino.






