L’Orforglipron, un innovativo agonista del recettore GLP-1 non peptidico, somministrabile per via orale
|
Getting your Trinity Audio player ready...
|
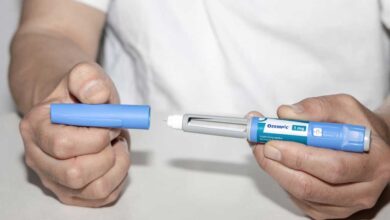
L’Orforglipron è un innovativo farmaco agonista del recettore del peptide-1 simile al glucagone (GLP-1, GLP-1 RA) non peptidico, sviluppato dall’azienda americana Eli Lilly che avrà il nome commerciale di Foundayo e che si pone come alternativa economica e di più facile somministrazione rispetto ai più noti Wegovy o Mounjaro.
L’Orforglipron è un farmaco particolarmente innovativo perché, pur essendo un agonista del recettore GLP-1 (come l’Ozempic o il Wegovy), è una piccola molecola non peptidica.
In dettaglio
- Gli agonisti del recettore del GLP-1 (GLP-1 RA) sono farmaci antidiabetici e per la gestione del peso che mimano l’ormone incretinico GLP-1, migliorando il controllo glicemico e favorendo la perdita di peso. I principali principi attivi includono semaglutide, liraglutide, dulaglutide, exenatide e tirzepatide.
- Questo ormone ha diverse funzioni: agisce sulle aree del cervello che percepiscono la fame, aumentando la sensazione di sazietà dopo i pasti; rallenta la digestione e con essa il rilascio di glucosio nel sangue dagli alimenti; aumenta il rilascio di insulina, ormone che permette alle cellule di assorbire e utilizzare il glucosio; e inibisce il rilascio di glucagone, un altro ormone che in caso di necessità aumenta i livelli di glucosio nel sangue.
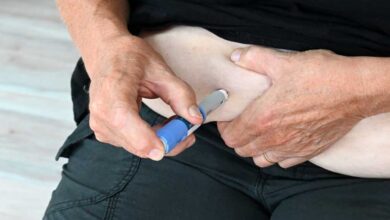
- I GLP-1AR sono farmaci a base peptidica che richiedono iniezioni sottocutanee. Attualmente, l’unico GLP-1RA orale approvato è una formulazione di semaglutide in compresse che, per essere assorbita, richiede di essere miscelata con un potenziatore dell’assorbimento gastrico: il salcaprozato di sodio. La compressa deve essere assunta a stomaco vuoto, almeno 30 minuti prima di mangiare o bere o assumere altri medicinali orali, e con non più di 120 ml di acqua. Nonostante queste accortezze, la formulazione orale di semaglutide ha una biodisponibilità compresa tra appena lo 0,4% e l’1,0%.
- L’Orforglipron appartiene a una nuova classe di GLP-1RA non peptidici orali, sintetizzati chimicamente. Orforglipron è un potente agonista parziale del recettore GLP-1 che, grazie una maggiore attivazione della via dell’AMPciclico (cAMP) rispetto al reclutamento della β-arrestina, potrebbe offrire una desensibilizzazione recettoriale inferiore rispetto agli agonisti completi del recettore GLP-1.
- Orforglipron, essendo una piccola molecola non proteica non prevede restrizioni sulla somministrazione di cibo o acqua.
- Questa caratteristica rappresenta una rivoluzione nel trattamento dell’obesità e del diabete di tipo 2, poiché permette di ottenere un’efficacia simile ai farmaci iniettabili (come Wegovy o Ozempic) attraverso una semplice somministrazione (una pillola) giornaliera.
- A differenza dei citati ben noti agonisti del recettore del GLP-1, che hanno una natura peptidica per cui non possono essere somministrati per via orale perché verrebbero distrutti dai succhi gastrici – ma richiedono il ricorso ad iniezioni (tranne il Rybelsus),
l’Orforglipron è una molecola somministrabile per via orale.
- La sua struttura chimica le permette di essere somministrata per via orale in una singola compressa giornaliera, senza necessitare di enhancers di assorbimento o restrizioni rigorose legate al cibo o all’acqua (es. digiuno), a differenza del semaglutide orale.
- La somministrazione orale del farmaco anziché tramite iniezione migliora indubbiamente l’aderenza del paziente alla terapia.
- Il suo utilizzo inoltre non ha restrizioni dietetiche, il che ne migliora anche la praticità.
- Essendo sintetizzato chimicamente e non tramite processi biotecnologici complessi, è potenzialmente più semplice ed economico da produrre su larga scala.
- Essendo una piccola molecola, è chimicamente più stabile e non richiede la catena del freddo, facilitando la conservazione e la distribuzione.
In sintesi, l’Orforglipron rappresenta un passo avanti nella terapia dell’obesità, offrendo la potenza di un GLP-1 iniettabile in una comoda formulazione in pillola.
- Risultati nella sperimentazione clinica: L’uso di Orforfglipron non ha comportato solamente la perdita di peso (mediamente attorno al 15% del peso corporeo iniziale in 36-72 settimane, in pazienti con obesità o sovrappeso) ma, come già visto con semaglutide, ha portato ad un miglioramento di tutti i parametri cardio metabolici e le condizioni correlate al peso prespecificate (ipertensione, dislipidemia, malattie cardiovascolari o sindrome ostruttiva delle apnee notturne).
Gli eventi avversi più comuni riportati con Orforfglipron sono stati eventi gastrointestinali, di entità da lieve a moderata e principalmente durante l’incremento della dose.
Il profilo di sicurezza di Orforfglipron è risultato coerente con quello della classe degli agonisti del recettore GLP-1. - Vantaggi: Oltre ad avere la stessa efficacia in termini di perdita di peso della semaglutide iniettiva (Wegovy) permette la somministrazione orale in compresse con enormi vantaggi sia in termini praticità e aderenza rispetto alle iniezioni sia di minori effetti collaterali (gastro-intestinali); inoltre non necessita della catena del freddo e si assume indipendentemente dai pasti.
- Effetti collaterali: Simili ad altri GLP-1 RA, gli effetti avversi più comuni sono di natura gastrointestinale, come nausea, diarrea e stitichezza.
- Stato attuale e disponibilità: Il 1 aprile 2026 la Food and Drug Admnistration, l’ente regolatore dei farmaci e dei prodotti alimentari negli Stati Uniti, ha approvato la vendita negli USA. La decisione è arrivata in tempi particolarmente rapidi grazie a un nuovo iter di approvazione, per ora in fase di sperimentazione, chiamato National Priority Voucher (CNPV), che accorcia notevolmente i tempi per i farmaci con un particolare profilo di necessità, riducendole a 50 giorni (una velocità che in parte preoccupa, per l’impossibilità di effettuare valutazioni approfondite). Con le procedure normali, l’agenzia avrebbe avuto tempo fino al gennaio 2027 per esprimersi.
- Indicazioni: Il farmaco potrà quindi essere prescritto alle persone obese che hanno almeno una condizione patologica associata come il diabete di tipo 2 o una malattia cardiaca o renale, in aggiunta a una dieta controllata e all’esercizio fisico. Proposto in compresse, Foundayo (questo il nome commerciale) può essere assunto in dosi crescenti da un minimo di 0,8 milligrammi (mg) al giorno fino a un massimo, per chi lo tollera, di 17,2 mg, ma solo dopo almeno un mese di dosaggi crescenti. Gli effetti collaterali sono quelli già noti con i farmaci iniettabili, e cioè soprattutto nausea, vomito, diarrea e altri disturbi gastrointestinali e altri tutti indicati nel foglietto, che contiene anche un avviso in evidenza relativo all’aumento del rischio di tumori tiroidei.
- Costo stimato: Negli USA, il prezzo previsto oscilla tra i 150 e i 350 dollari al mese a seconda del dosaggio, rendendolo potenzialmente più economico rispetto alle versioni iniettabili. Al momento (aprile 2026), l’Orforglipron non è ancora disponibile in commercio in Italia per cui non ha un prezzo ufficiale di vendita ma è in attesa dell’approvazione finale da parte dell’Agenzia Europea per i Medicinali (EMA) e della successiva negoziazione con l’AIFA. Si prevede che, una volta approvato, possa essere a carico del paziente (fascia C) se prescritto per il controllo del peso (obesità), similmente ad altri farmaci simili già approvati.
Wharton S, Aronne LJ, Stefanski A, Alfaris NF, Ciudin A, Yokote K, Halpern B, Shukla AP, Zhou C, Macpherson L, Allen SE, Ahmad NN, Klise SR; ATTAIN-1 Trial Investigators. Orforglipron, an Oral Small-Molecule GLP-1 Receptor Agonist for Obesity Treatment. N Engl J Med. 2025 Nov 6;393(18):1796-1806. doi: 10.1056/NEJMoa2511774. Epub 2025 Sep 16. PMID: 40960239. Horn DB, Ryan DH, Kis SG, Alves B, Mu Y, Kim SG, Aberle J, Bain SC, Allen S, Sarker E, Wu Q, Stefanski A, Jouravskaya I; ATTAIN-2 Trial Investigators. Orforglipron, an oral small-molecule GLP-1 receptor agonist, for the treatment of obesity in people with type 2 diabetes (ATTAIN-2): a phase 3, double-blind, randomised, multicentre, placebo-controlled trial. Lancet. 2026 Dec 20;406(10522):2927-2944. doi: 10.1016/S0140-6736(25)02165-8. Epub 2025 Nov 20. PMID: 41275875.