Regolatori dell’espressione genica – le metiltransferasi

|
Getting your Trinity Audio player ready...
|
L’alimentazione è un determinante modificabile della durata della salute e del rischio di malattia. Nell’ultimo decennio, il campo dell’epigenetica nutrizionale ha cominciato a dare spiegazioni su come componenti della dieta influenzino l’espressione genica e la funzione cellulare senza alterare la sequenza del DNA.
La metilazione del DNA è una delle modifiche epigenetiche più ampiamente studiate; essa comporta l’aggiunta di un gruppo metilico ai residui di citosina all’interno dei siti CpG. Questa reazione è catalizzata dalle DNA metiltransferasi (DNMT) ed è essenziale per la stabilità del genoma, il silenziamento genico e la differenziazione cellulare, e la sua disregolazione; modelli aberranti di metilazione del DNA sono stati implicati nel cancro, nella neurodegenerazione, nelle malattie cardiovascolari e metaboliche e nei disturbi legati all’età.
- Che cosa sono le metiltransferasi
Le metiltransferasi sono una classe di enzimi che trasferiscono un gruppo metile (–CH₃) da una molecola donatrice (di solito la S-adenosilmetionina, SAM) ad altre molecole biologiche (a substrati come DNA, RNA, proteine o piccoli composti).
Questo processo si chiama metilazione ed è una delle principali modificazioni epigenetiche, cioè regolazioni dell’espressione genica che non cambiano la sequenza del DNA ma ne influenzano il funzionamento.
In pratica:
👉 Le metiltransferasi sono “interruttori biochimici” che regolano quali geni vengono attivati o silenziati.
Giocano un ruolo cruciale nell’epigenetica regolando l’espressione genica tramite la metilazione e nel metabolismo di farmaci.
- Tipi principali di metiltransferasi
- a) DNA metiltransferasi (DNMT): Aggiungono gruppi metilici alla citosina nel DNA (isole CpG), solitamente reprimendo la trascrizione genica e silenziando i geni. Sono fondamentali per lo sviluppo embrionale, l’invecchiamento e l’infiammazione.
| · DNMT1 → mantiene i pattern di metilazione durante la replicazione cellulare. Riconoscono i siti CpG metilati solo sul filamento stampo e metilano il corrispondente filamento appena sintetizzato, garantendo la trasmissione del pattern di metilazione alle cellule figlie.
· DNMT3A e DNMT3B → creano nuove metilazioni (metilazione “de novo”), durante lo sviluppo embrionale e il differenziamento cellulare · DNMT3L: Pur non avendo attività catalitica propria, funge da cofattore essenziale per potenziare l’azione delle altre DNMT3. Queste agiscono soprattutto su sequenze di DNA chiamate isole CpG, ricche di citosina e guanina. |
Esistono due classi principali di DNMT: le metiltransferasi di mantenimento, principalmente DNMT1, che assicurano la fedele eredità dei modelli di metilazione durante la replicazione del DNA, e le metiltransferasi de novo, DNMT3A e DNMT3B, che stabiliscono nuovi modelli di metilazione durante lo sviluppo precoce.
Sebbene gli enzimi de novo siano per lo più attivi durante l’embriogenesi, prove emergenti suggeriscono che mantengano un’attività residua nei tessuti somatici adulti, contribuendo al continuo rimodellamento epigenetico per tutta la durata della vita. La modulazione dell’attività DNMT è quindi di notevole interesse per l’identificazione di strategie nutrizionali volte a rallentare l’invecchiamento epigenetico e promuovere traiettorie di invecchiamento sane.
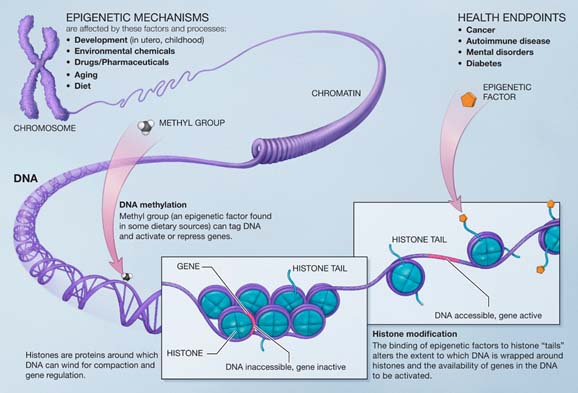
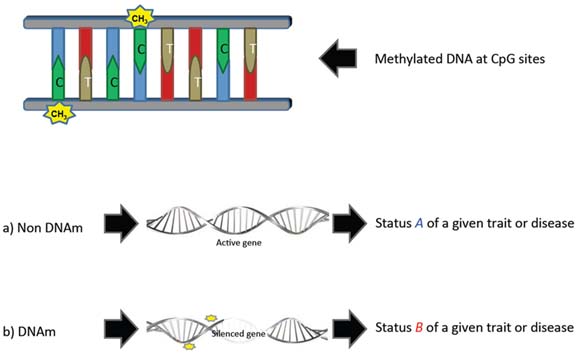
Prove recenti suggeriscono che i composti bioattivi dietetici possono influenzare la metilazione del DNA agendo come inibitori naturali della DNMT, modulando i marcatori epigenetici e influenzando così la durata della salute e la suscettibilità alle malattie.
Polifenoli, flavonoidi, isotiocianati e altri metaboliti derivati dalle piante hanno dimostrato effetti diretti e indiretti sull’attività della DNMT, portando a cambiamenti globali o specifici del locus nei modelli di metilazione del DNA. Ad esempio, è stato dimostrato che l’epigallocatechina gallato (EGCG) dal tè verde, la genisteina (GE) dalla soia, la curcumina (CU) dalla curcuma e il resveratrolo dall’uva riducono l’ipermetilazione mediata dalla DNMT, riattivando così i geni oncosoppressori e modulando le vie infiammatorie. Inoltre, nutrienti come folato, colina, betaina e vitamine B2, B6 e B12 regolano l’attività DNMT attraverso la modulazione della S-adenosil-L-metionina, il donatore di metile universale nelle reazioni di metilazione del DNA. L’ipometilazione globale e l’ipermetilazione sito-specifica contribuiscono all’instabilità genomica, all’infiammazione e alla senescenza cellulare, suggerendo che i modulatori DNMT dietetici possono avere un ruolo cruciale nel rallentare l’invecchiamento epigenetico.
Ricerche emergenti evidenziano la stretta interconnessione tra dieta, microbioma intestinale e meccanismi epigenetici, evidenziando come i metaboliti microbici influenzino la disponibilità dei donatori di metile e la regolazione del DNMT, modellando così i paesaggi epigenomici associati all’età. Oltre al cancro, le alterazioni nella metilazione del DNA sono ora riconosciute come segni distintivi dell’invecchiamento. Queste modifiche in specifici siti CpG associati all’età vengono utilizzate nel calcolo dell’età di metilazione del DNA (DNAmAge), un predittore affidabile dell’invecchiamento biologico e biomarcatore delle malattie legate all’et]. Pertanto diventa fattibile intervenire con la dieta per mitigare l’invecchiamento epigenetico.
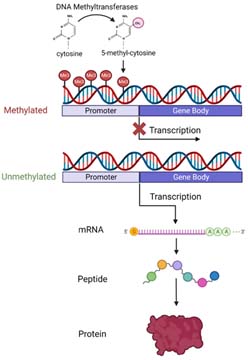 Le isole CpG sono regioni del DNA, lunghe solitamente più di 200 paia di basi, caratterizzate da un’alta concentrazione di dinucleotidi citosina-guanina (CpG) rispetto al resto del genoma. Situate spesso nei promotori dei geni, vicino al sito d’inizio della trascrizione, specialmente nei geni housekeeping. agiscono come regolatori dell’espressione genica; la loro metilazione spegne i geni, mentre la mancanza di metilazione ne permette l’attivazione. La metilazione delle citosine nelle isole CpG è una modifica epigenetica chiave che influenza la struttura della cromatina e l’accessibilità ai fattori di trascrizione. Queste regioni sono cruciali per la regolazione dell’identità cellulare e la stabilità del genoma.
Le isole CpG sono regioni del DNA, lunghe solitamente più di 200 paia di basi, caratterizzate da un’alta concentrazione di dinucleotidi citosina-guanina (CpG) rispetto al resto del genoma. Situate spesso nei promotori dei geni, vicino al sito d’inizio della trascrizione, specialmente nei geni housekeeping. agiscono come regolatori dell’espressione genica; la loro metilazione spegne i geni, mentre la mancanza di metilazione ne permette l’attivazione. La metilazione delle citosine nelle isole CpG è una modifica epigenetica chiave che influenza la struttura della cromatina e l’accessibilità ai fattori di trascrizione. Queste regioni sono cruciali per la regolazione dell’identità cellulare e la stabilità del genoma.
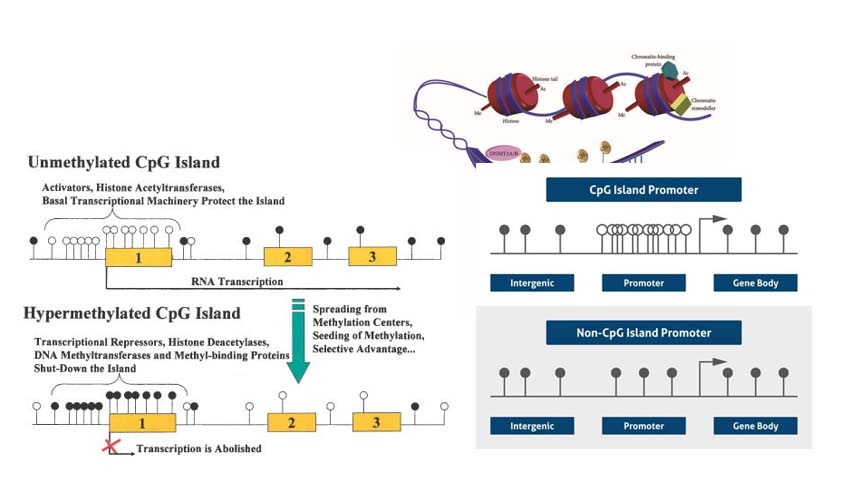
- b) Istone metiltransferasi: modificano le proteine istoniche attorno alle quali è avvolto il DNA, influenzando:
- la compattezza della cromatina
- l’accessibilità dei geni
- c) Metiltransferasi su RNA e proteine
Hanno ruoli nella:
- regolazione della traduzione proteica
- risposta allo stress
- modulazione immunitaria
Esempi includono la catecol-O-metiltrasferasi (COMT) che degrada i neurotrasmettitori, e la tiopurina metiltransferasi (TPMT) coinvolta nel metabolismo di farmaci immunosoppres-sori.
Importanza Biologica: Regolano l’invecchiamento biologico, l’imprinting genomico e la stabilità del genoma. Un malfunzionamento è spesso associato allo sviluppo di tumori.
Questi enzimi sono studiati come bersagli terapeutici nel cancro per la loro capacità di riattivare geni soppressi.
- Come operano le DNA metiltransferasi
Il meccanismo è relativamente semplice:
- L’enzima riconosce una sequenza specifica nel DNA.
- Trasferisce un gruppo metile alla citosina.
- Questo modifica la struttura del DNA.
- Le proteine che attivano i geni non riescono più a legarsi.
👉 Risultato:
Il gene viene spento o ridotto nella sua espressione.
Questo processo è fondamentale per:
- sviluppo embrionale
- differenziazione cellulare
- controllo dei tumori
- regolazione dell’infiammazione
La metilazione agisce pertanto come “interruttore” epigenetico: un’ipermetilazione (eccessiva) spesso spegne geni oncosoppressori, mentre una ipometilazione può attivarli.
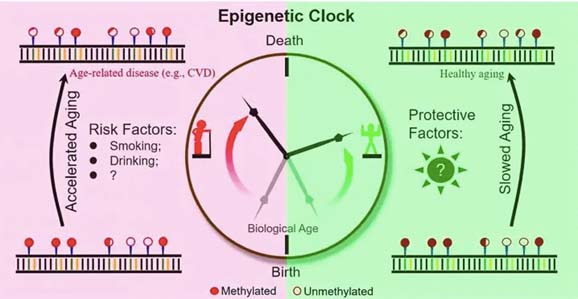
- Epigenetica e invecchiamento biologico
Il 70% della tua longevità dipende da te. Solo il restante 30% è scritto nei geni. Questa consapevolezza – scientificamente provata – ci invita a spostare lo sguardo: non possiamo cambiare la nostra genetica, ma possiamo intervenire attivamente su ciò che la influenza, grazie all’epigenetica. Questa ha rivoluzionato il nostro modo di comprendere la salute, svelando il continuo dialogo tra il nostro DNA e l’ambiente. Una scoperta che cambia le regole del gioco, perché ci offre una verità potente: ogni giorno possiamo fare scelte che lasciano un’impronta positiva nel nostro futuro biologico.
L’epigenetica regola l’invecchiamento biologico modificando l’espressione genica senza alterare il DNA, accumulando cambiamenti (come la metilazione) influenzati da stile di vita e ambiente. Questi marcatori formano “orologi epigenetici” che misurano l’età biologica, spesso diversa da quella anagrafica, permettendo potenzialmente di rallentare o invertire l’invecchiamento cellulare tramite dieta, attività fisica e riduzione dello stress.
Con l’età, tuttavia, l’epigenoma va incontro a quella che viene definita deriva epigenetica, ovvero accumula modificazioni casuali (metilazione del DNA, modifiche istoniche) che alterano la funzione genica, portando all’invecchiamento dei tessuti e malattie correlate.
Caratteristiche:
- perdita della precisione dei pattern di metilazione
- ipometilazione globale del DNA
- ipermetilazione di geni specifici (es. antinfiammatori o riparativi)
Questo contribuisce alla cosiddetta:
| Il drift epigenetico (o deriva epigenetica) è il progressivo accumulo, legato all’età, di modificazioni epigenetiche stocastiche (casuali) all’interno del genoma di un organismo. Queste variazioni non alterano la sequenza del DNA (i geni stessi), ma modificano le modalità di “lettura” dei geni (ad esempio tramite metilazione del DNA o modifiche istoniche), influenzando l’espressione genica e la funzione cellulare nel corso della vita.
Il drift epigenetico · è guidato da una combinazione di errori casuali nel mantenimento dei marchi epigenetici durante la divisione cellulare e l’influenza di fattori esterni come l’ambiente, lo stile di vita, l’alimentazione, lo stress e l’inquinamento.
In sintesi, il drift epigenetico rappresenta il “disordine” epigenetico che aumenta nel tempo, rendendo le cellule meno efficienti e più inclini a malfunzionamenti, rappresentando una delle cause molecolari dell’invecchiamento. |
👉 “firma epigenetica dell’invecchiamento”, su cui si basano gli orologi epigenetici
- Orologi Epigenetici: Strumenti come gli algoritmi di Horvath, Hannum, PhenoAge e GrimAge stimano la velocità di invecchiamento, aiutando a monitorare l’efficacia di interventi anti-age.
- Età Cronologica vs Biologica: L’età cronologica è il tempo vissuto; l’età biologica (o epigenetica) misura lo stato di usura cellulare. Un’età epigenetica più alta di quella cronologica indica un invecchiamento accelerato, associato a un maggior rischio di malattie croniche.
- Fattori Influenzanti: L’invecchiamento epigenetico è guidato da fattori ambientali ed esposizioni (esposoma). Il fumo è il principale responsabile dell’invecchiamento, seguito da alcol e cattiva alimentazione.
- Reversibilità e Stile di Vita: L’epigenetica offre l’opportunità di influenzare il proprio destino biologico. Scelte salutari come una dieta corretta, attività fisica e la cessazione del fumo possono ridurre l’età biologica e l’infiammazione.
- Disregolazione delle DNMT nell’invecchiamento
Con il tempo:
- l’attività delle DNMT diventa meno efficiente e meno coordinata.
- aumenta lo stress ossidativo e metabolico.
- si altera la disponibilità dei donatori di metile (es. SAM).
Conseguenze principali:
1) Instabilità genomica
La perdita di metilazione globale:
- aumenta mutazioni e danni al DNA
- attiva sequenze genetiche silenti (retrotrasposoni)
| La disregolazione delle DNA metiltransferasi (DNMT) è un meccanismo chiave nell’invecchiamento epigenetico, caratterizzato da alterazioni nella metilazione del DNA che influenzano l’espressione genica, la stabilità genomica e la funzione cellulare. Con l’avanzare dell’età, si osserva un complesso cambiamento che include una generale ipometilazione genomica (perdita di gruppi metilici) e una ipermetilazione specifica in alcune aree, in particolare a livello dei promotori genici. In particolare, la DNMT1, enzima responsabile del mantenimento dei pattern di metilazione durante la divisione cellulare, tende a diminuire con l’età. Questo calo contribuisce alla ipometilazione globale, portando all’attivazione di geni precedentemente silenziati e all’instabilità genomica. Mentre la DNMT1 diminuisce, si osserva spesso un aumento o una disregolazione delle DNMT de novo (DNMT3A e DNMT3B) con l’invecchiamento. Questa alterazione contribuisce all’ipermetilazione focale delle CpG island nei promotori, che spesso porta al silenziamento di geni oncosoppressori o geni coinvolti nel mantenimento cellulare. |
Questo accelera l’invecchiamento cellulare.
L’invecchiamento è pertanto associato a una ridotta metilazione nelle regioni eterocromatiche, come le sequenze ripetute e i trasposoni, riducendo la stabilità del genoma. La disregolazione delle DNMT porta a un “drift” epigenetico (deriva epigenetica), che altera le risposte allo stress, aumenta l’infiammazione cronica (inflammaging) e riduce la funzionalità dei tessuti, contribuendo a malattie legate all’età come il cancro, l’osteoartrosi e le malattie neurodegenerative. Queste alterazioni delle DNMT sono fondamentali per la formazione degli “orologi epigenetici” o orologi di metilazione del DNA, utilizzati per misurare l’età biologica rispetto a quella cronologica.
6) Senescenza cellulare
La senescenza cellulare è un processo fisiologico irreversibile in cui le cellule diventano “anziane”, smettono di dividersi ma rimangono metabolicamente attive e cominciano a produrre specifiche molecole che richiamano il sistema immunitario alla loro eliminazione e alla loro sostituzione con nuove cellule “fresche”, in grado di replicarsi e compiere il loro lavoro, fungendo da meccanismo di protezione contro i tumori.
Non sempre però la senescenza cellulare è un processo fisiologico. È stato infatti scoperto che alcuni virus possono innescare la senescenza precoce delle cellule colpite come conseguenza dello stress subìto.
Questo è stato osservato soprattutto nei tessuti più colpiti dal virus (soprattutto nasofaringe e polmone) dove le cellule invecchiate rilasciano sostanze pro-infiammatorie, proteine SASP (Senescent Associated Secreted Phenotype), che alterano il microambiente circostante e danneggiano le cellule sane vicine, con forte attivazione della cascata infiammatoria. Con l’avanzare dell’età però l’efficienza dei processi immunitari per l’eliminazione delle cellule senescenti si riduce, per cui queste vanno ad accumularsi in tessuti dell’organismo, che possono favorire malattie legate all’avanzare dell’età, come gli stessi tumori oppure stati d’infiammazione cronica.
Al presente, la ricerca si concentra sullo sviluppo di senolitici, sostanze in grado di eliminare selettivamente le cellule senescenti, o senomorfici, che riducono il rilascio di molecole infiammatorie da parte di tali cellule, per ritardare le malattie legate all’età.
- DNMT, alterazione del metabolismo e infiammazione cronica di basso grado (inflammaging)
DNMT influenzano geni legati a:
- metabolismo energetico
- funzione mitocondriale
- risposta allo stress
Questo contribuisce alla fragilità dell’organismo
Grassi alimentari e obesità influenzano i meccanismi DNMT, in particolare nei macrofagi del tessuto adiposo (ATM), modificando la loro polarizzazione verso un fenotipo infiammatorio.
Risposte infiammatorie croniche, come quelle indotte dal fumo o da cattiva alimentazione, creano un ambiente in cui le DNMT modificano il paesaggio epigenetico.
Le alterazioni indotte dalle DNMT contribuiscono a una risposta infiammatoria silente ma sistemica che riduce le funzioni immunitarie e colpisce l’apparato vascolare e metabolico
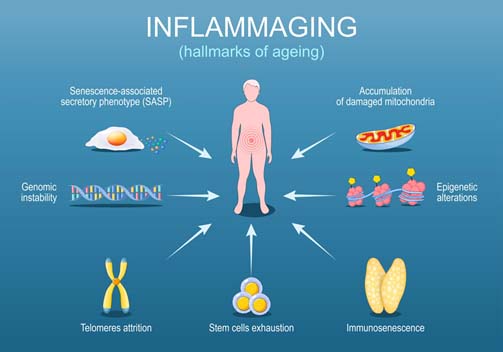
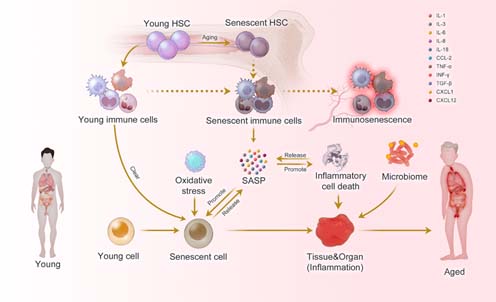
L’inflammaging è un processo di infiammazione cronica, asintomatica e di basso grado che si sviluppa con l’avanzare dell’età, agendo come un “regista silenzioso” dell’invecchiamento. Si caratterizza per un aumento sistemico di citochine pro-infiammatorie in assenza di infezioni, accelerando il declino funzionale e il rischio di malattie croniche.
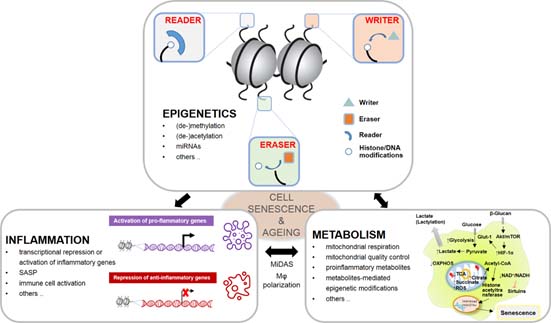
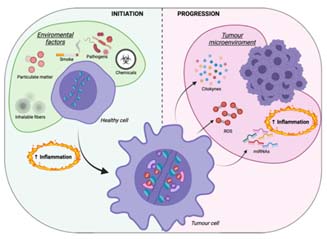
L’invecchiamento è associato a una infiammazione sistemica lieve ma persistente:
👉 inflammaging.
La disregolazione delle DNMT contribuisce attraverso diversi meccanismi.
- a) Attivazione di geni pro-infiammatori
Una ridotta metilazione di:
- TNF-α
- IL-6
- NF-kB
porta a una maggiore produzione di citochine infiammatorie.
Questo crea:
- un circolo vizioso tra infiammazione e alterazioni epigenetiche.
- b) Alterazioni del sistema immunitario
Si osservano:
- immunosenescenza
- squilibrio tra cellule pro e anti-infiammatorie.
Le DNMT influenzano:
- differenziazione dei linfociti
- risposta immunitaria.
- c) Influenza dello stile di vita
Fattori che modificano l’attività delle DNMT:
- dieta povera di nutrienti metilanti
- stress cronico
- sedentarietà
- disbiosi intestinale
- esposizione a inquinanti.
Nutrienti chiave:
- folati
- vitamina B12
- colina
- betaina
- metionina.
Ovviamente, il microbiota, che produce metaboliti utili per la regolazione epigenetica e immunitaria, svolge un ruolo fondamentale.
- d) Stress ossidativo e mitocondri
Lo stress ossidativo:
- altera la funzione delle DNMT
- modifica il metabolismo della SAM.
Questo contribuisce all’infiammazione cronica.
- Implicazioni pratiche per prevenzione e salute
Questo punto è strategico: la regolazione epigenetica è modificabile, quindi:
👉 l’invecchiamento biologico non è totalmente programmato.
Interventi utili:
- alimentazione ricca di polifenoli e fibre
- sostegno al microbiota
- esercizio fisico
- sonno regolare
- gestione dello stress.
Alcuni composti naturali modulano le DNMT:
- resveratrolo
- curcumina
- catechine del tè verde.
- Sintesi e conclusioni
Le DNA metiltransferasi sono enzimi che regolano l’attività dei geni attraverso la metilazione del DNA. Con l’invecchiamento questi sistemi diventano meno precisi, favorendo:
- instabilità genetica
- infiammazione cronica
- senescenza cellulare
- malattie legate all’età.
Stile di vita e alimentazione influenzano direttamente questi processi, rendendo possibile rallentare l’invecchiamento biologico.
- l’alimentazione non nutre solo il corpo, ma anche i batteri intestinali;
- il microbiota influenza l’infiammazione, l’invecchiamento e la salute;
- attraverso lo stile di vita si possono “attivare o spegnere” meccanismi protettivi.
Campisi M, Cannella L, Visioli F, Pavanello S. A Systematic Review of Food-Derived DNA Methyltransferase Modulators: Mechanistic Insights and Perspectives for Healthy Aging. Adv Nutr. 2025 Nov;16(11):100521. doi: 10.1016/j.advnut.2025.100521. Epub 2025 Sep 18. PMID: 40975498; PMCID: PMC12554032.


